CONCEPTO
La fibrilación auricular (FA) es la arritmia cardiaca más frecuente en la práctica clínica. Puede tener consecuencias deletéreas sobre la función cardiaca (caída del gasto cardiaco debido a la disminución del tiempo de llenado ventricular por la frecuencia ventricular rápida de un lado, y la pérdida de la contribución auricular al llenado ventricular por otro) y aumenta el riesgo de embolia sistémica (asociación fuerte a infarto cerebral embólico). Incluso, la taquiarrítmia crónica puede desarrollar cardiomiopatía relacionada con taquicardia.
Mecanismos de producción.
En la génesis de la FA intervienen múltiples factores de carácter anatómico y funcional que condicionan la aparición de las anormalidades electro-fisiológicas que favorecen la instalación y la perpetuación de la arritmia. Los mecanismos electro-fisiológicos básicos de la FA son la reentrada y las descargas rápidas de focos auriculares ectópicos. Se han señalado otros disparadores arritmogénicos como el sistema nervioso autónomo (fundamentalmente el vago) y la asociación al síndrome de Wolff-Parkinson-White (S-WPW).
Causas y factores potenciadores de FA:
Cardiovasculares:
1. Aumento de la presión auricular:
• Enfermedad valvular mitral o tricúspide.
• Enfermedad de las válvulas semilunares potenciadoras de hipertrofia ventricular.
• Hipertensión sistémica o pulmonar.
• Enfermedad miocárdica primaria o secundaria, que conduce a disfunción diastólica o sistólica.
• Tumores o trombos intracardiacos.
2. Enfermedad auricular inflamatoria o infiltrativa:
• Pericarditis.
• Amiloidosis.
• Miocarditis.
• Fibrosis auricular inducida por la edad.
3. Enfermedades cardiacas congénitas:
4. Cirugía cardiaca.
5. Isquemia auricular: enfermedad arterial coronaria.
6. Fibrilación auricular idiopática (aislada).
No cardiovasculares:
1. Tóxicos (tabaco, alcohol, cafeína, cocaína, anfetaminas).
2. Trastornos endocrinos: Hipertiroidismo, feocromocitoma.
3. Trastornos del equilibrio hidroelectrolítico y ácido-básico.
4. Alteraciones del tono autonómico: aumento de la actividad simpática o parasimpática.
5. Neurogénico: Hemorragia subaracnoidea y accidentes cerebrovascualares no hemorrágicos.
6. Postoperatorio de cirugía pulmonar o esofágica.
DIAGNÓSTICO
Características clínicas.
Anamnesis: La forma paroxística cursa con palpitaciones de comienzo súbito, y puede existir repercusión hemodinámica: disnea de distinto grado, angina, síncope u otros según la enfermedad de base. La manifestación inicial de la FA puede ser resultado de complicaciones embólicas o síntomas de insuficiencia cardiaca.
Los pacientes con FA permanente suelen estar asintomáticos.
Exploración física: pulso irregular (rápido, normal o lento) de amplitud variable, ruidos cardiacos arrítmicos, variación en la intensidad del primer ruido cardiaco, discordancia entre frecuencia apical y radial, ausencia de onda a de pulso venoso yugular, signos de deterioro hemodinámico, signos de la enfermedad concomitante, signos de embolia sistémica.
Características electrocardiográficas.
• Ausencia de ondas P, reemplazadas por despolarizaciones auriculares rápidas, desorganizadas, que se traducen en oscilaciones de la línea de base (ondas f), de morfología variable (finas, gruesas, a veces casi imposibles de identificar) con una frecuencia mayor a 350 latidos/min.
• Respuesta ventricular irregular (ciclo R-R constantemente variable). Si la frecuencia ventricular (FrV) es rápida oscila generalmente entre 120 y 160 latidos/min. Si la FrV es muy rápida o muy lenta la irregularidad R-R es menos evidente.
• Los complejos QRS son habitualmente de morfología normal pero puede haber latidos con grados intermedios de aberración o totalmente aberrantes (frecuentemente con morfología de bloqueo de rama derecha, aberración Ashman). De igual forma QRS anchos que recuerdan la taquicardia ventricular polimórfica están presentes en la FA asociada al S-WPW.
• Pueden existir anormalidades de ST-T que pueden deberse meramente a la respuesta ventricular rápida o también a efecto digital o a cardiopatía subyacente.
Clasificación.
No existe acuerdo en la clasificación ni en la terminología utilizada para caracterizar a la FA, especialmente su patrón temporal. En la literatura actual, la FA generalmente se divide en dos formas: paroxística y crónica o permanente. La siguiente clasificación fue propuesta por Sopher y Camm y aceptada por el grupo de trabajo de arritmias de la Sociedad Europea de Cardiología por su utilidad en la práctica clínica.
• FA paroxística: episodios de menos de 48 horas de duración, suelen ser autolimitados.
• Persistente: episodios no autolimitados de más de 48 horas de duración.
• Permanente o crónica: el restablecimiento del ritmo sinusal no ha sido posible o no se considera indicado.
• FA de reciente diagnóstico: término utilizado para referirse a la FA que se diagnostica sin que el paciente pueda precisar el tiempo desde el inicio de la arritmia.
Tanto los episodios paroxísticos como los persistentes pueden manifestarse de forma recurrente.
Estudios rutinarios a realizar.
Los estudios van encaminados a evaluar los factores etiológicos, fisiopatológicos y clínicos que se asocian a la FA y que determinan su manejo terapéutico.
1. Electrocardiograma.
• Valoración de la frecuencia ventricular.
• Presencia de hipertrofia ventricular izquierda o derecha.
• Presencia de signos de isquemia- infarto.
• Trastornos de la conducción intraventricular (bloqueos de rama).
• Duración y morfología de la onda p en ritmo sinusal.
• Pre excitación
2- Analítica general.
• Hemograma completo.
• Glucemia.
• Lipidograma completo.
• Creatinina
• Ionograma.
3- Ecocardiograma (ECG) transtorácico: evaluar tamaño de aurícula izquierda y derecha, dimensiones y función del ventrículo izquierdo, presiones pulmonares, trombo en aurícula izquierda (baja sensibilidad), enfermedad pericárdica.
4-Radiografía de tórax.
5-Prueba de esfuerzo: reproducir FA inducida por el esfuerzo, evaluar control adecuado de la FC en la FA permanente.
6-Ecocardiograma transesofágico: para descartar trombo en la aurícula izquierda en la FA de más de 48 horas, cuando se opta por la cardioversión.
En ausencia de ecocardiograma se puede estimar con alta probabilidad que un paciente no es portador de una cardiopatía significativa cuando son normales los siguientes parámetros:
• Anamnesis detallada: ausencia de clínica cardiológica previa y de episodios de insuficiencia cardiaca congestiva (ICC).
• Exploración física cardiológica normal.
• ECG: se valorara especialmente la presencia de signos de necrosis, bloqueos de rama, alteraciones de la repolarización y crecimiento de cavidades.
• Radiografía de tórax: sin hallazgos desde el punto de vista cardiológico.
Ante la anomalía de cualquiera de estos parámetros, se priorizará la seguridad del paciente y se atenderá como si tuviera una cardiopatía estructural significativa.
TRATAMIENTO
Servicio de Urgencias.
FA paroxística o aguda (menos de 48 horas):
• Máxima prioridad, código rojo.
• Reposo horizontal.
• Traslado del paciente a la UCIE.
• Acceso intravenoso periférico.
• Oxígeno por catéter nasal a 4 litros por minuto.
• Evaluación inicial dirigida a: Valoración del estado hemodinámica, identificación y corrección de circunstancias precipitantes reversibles: fiebre, infección, toxicidad, disfunción del ventrículo izquierdo (VI), inflamación cardiaca (carditis, pericarditis), embolia pulmonar, enfermedad pulmonar obstructiva crónica (EPOC) descompensada, tirotoxicosis, trastornos del equilibrio hidroelectrolítico y ácido-básico, así como valoración de la probabilidad de restaurar el ritmo sinusal (RS).
El tratamiento a elegir dependerá de la hemodinámica. Si hemodinámica inestable cardioversión eléctrica (choque sincrónico con 300 J), en caso de disponer de desfibrilador bifásico se puede comenzar con 100 J. En pacientes con hemodinámica estable, control de la respuesta ventricular con fármacos o cardioversión.
La cardioversión a ritmo sinusal puede hacerse eléctrica o farmacológica, considerándose candidatos a la cardioversión todos los pacientes con FA de reciente comienzo y de reciente diagnóstico. No obstante, no siempre es posible conseguir el ritmo sinusal, bien porque la cardioversión es inefectiva, o porque se produce una recaída precoz en FA.
Marcadores clínicos de riesgo de cardioversión inefectiva:
• Edad superior a los 75 años.
• Duración de los episodios de FA de más de un año.
• Tamaño de la aurícula izquierda superior a 55 mm.
Marcadores clínicos de riesgo de recidiva precoz de la FA:
• Enfermedad valvular mitral.
• Larga evolución de la arritmia, más de un año.
• Tamaño de la aurícula izquierda superior a 55 mm.
• Antecedentes de al menos dos cardioversiones eléctricas o de fracaso de al menos dos fármacos antiarrítmicos.
• VI dilatado y/o fracción de eyección deprimida (menos de 40 %).
• Antecedentes de recidiva precoz (menos de un mes).
Cardioversión eléctrica no indicada si:
• Alteraciones electrolíticas o de gases sanguíneos.
• Sospecha de intoxicación digital.
• Sospecha de enfermedad del seno.
• Respuesta ventricular lenta.
• Alto riesgo de recurrencia.
• EPOC descompensada o embolia pulmonar.
• Procesos inflamatorios agudos del corazón.
Estos marcadores son orientativos y no tienen por sí solos suficiente peso clínico para contraindicar de forma absoluta un intento de cardioversión. La decisión debe ser particular en cada caso.
Razones para restaurar el RS en pacientes con FA:
• Regular el ritmo cardiaco.
• Restaurar la contribución auricular al grupo sanguíneo (GC).
• Mejorar la hemodinamia.
• Normalizar o mejorar el ambiente electrofisiológico.
• Prevenir la dilatación auricular.
• Prevenir la disfunción ventricular.
• Control fisiológico y adecuado de la frecuencia cardiaca (FC).
• Mejorar la calidad de vida mediante el alivio de los síntomas.
• Reducir las complicaciones tromboembólicas.
En pacientes inestables desde el punto de vista hemodinámico la elección es la cardioversión eléctrica que se realizará de urgencia en la UCIE; después se trasladará el paciente a la unidad de cuidados integrales del corazón, a la sección de terapia intensiva.
En los pacientes que se decida la cardioversión farmacológica, si no tienen enfermedad estructural cardiovascular se comenzará la medicación (con flecainida, propafenona o quinidal) y se ingresarán en el centro de dolor torácico (CDT) por 24 horas. Si presentan cardiopatía estructural se usará amiodarona en la UCIE y se ingresarán en la unidad de cuidados integrales al corazón en la sección de terapia intermedia.
Tratamiento farmacológico.
En pacientes hemodinámicamente estables se puede optar por la cardioversión farmacológica, previa disminución de la respuesta ventricular:
Control de la respuesta ventricular: el paso siguiente se dirige a la reducción de la respuesta ventricular (objetivo de 60-100 latidos/min) ello se logra más rápidamente con bloqueadores beta-adrenérgicos (especialmente en situaciones de tono simpático alto como IMA, embolia pulmonar, pericarditis) y con anticálcicos no dihidropiridinicos teniendo en cuenta el factor disfunción ventricular y la hipotensión. Muy útiles si ventrículos de pobre distensibilidad.
Los digitales se usan más, pero su efecto es más tardío y no son de elección si tirotoxicosis o ventrículos de pobre distensibilidad.
Dosis:
Digoxina intravenosa: 8-15 mcg/Kg (0,5-1 mg en pacientes de 70 Kg). La mitad de la dosis de inicio y resto a las 4 horas si es necesario.
Propranolol intravenoso: 1 mg repetible cada 5 min hasta 3 mg.
Metoprolol intravenoso: 2,5-5 mg cada 2-5 min hasta 15 mg.
Atenolol intravenoso: 2,5-5 mg en dos minutos hasta 10 mg en 10-15 min.
Verapamilo intravenoso: 0,075-0,15 mg/Kg (5-10 mg) en 2 min que puede repetirse a los 30 min.
Diltiazem intravenoso: 0,25-0,30mg /Kg (aproximadamente 20 mg).
Fármacos para lograr la reversión a ritmo sinusal:
Drogas de la clase I-C:( no si ICC o IM previo): Propafenona 600 mg vía oral dosis única, o glecainida 300 mg vía oral, dosis única.
Ambas pueden usarse por vía intravenosa a 2 mg/Kg/dosis.
Nivel de recomendación: I; Nivel de evidencia: A
Drogas de la clase III: Amiodarona, dosis de carga a 5 mg/kg y mantener a10 mg/kg en 24 horas. No debe utilizarse cuando se requiera una conversión rápida a ritmo sinusal.
Nivel de recomendación: IIa; Nivel de evidencia: A.
Drogas de clase I-A: Sulfato de quinidina 200-400 mg cada 4-6 horas vía oral durante 24-36 Procainamida por vía intravenosa, 100mg cada 5-10 minutos, sin pasar de 1 gramo.
Nivel de recomendación: IIb; Nivel de evidencia: C.
Si no se obtiene éxito y se sigue considerando la restauración del RS, sobre todo por bajo riesgo de recurrencia, se procederá con cardioversión eléctrica y se ingresará en la sección de terapia intermedia. En caso contrario, aceptar la arritmia e ingresar en la sección de terapia intermedia o sala convencional de cardiología. No es recomendable el uso combinado de fármacos antiarrítmicos, es preferible optar por la cardioversión eléctrica (CVE) electiva cuando fracasa el tratamiento con uno de los fármacos.
Si el paciente revierte es importante el mantenimiento del ritmo sinusal, la terapia farmacológica está indicada en pacientes con más de un episodio en tres meses, repercusión hemodinámica, episodios muy sintomáticos o en aquellos con patologías que predispongan a las recurrencias.
Los fármacos útiles son los del grupo IC (propafenona, flecainida) y los del III (amiodarona y sotalol). En estudios controlados, la eficacia de la propafenona, flecainida y sotalol es muy similar; la amiodarona parece ser algo más efectiva.
La elección del fármaco debe tener en cuenta sus propiedades farmacodinámicas y la presencia de cardiopatía estructural.
1. Ausencia de cardiopatía orgánica: Propafenona o flecainida, asociada a un fármaco que controle la respuesta ventricular en caso de recaída (beta-bloqueadores, o antagonistas del calcio) para evitar el riesgo de aparición de flúter auricular con conducción 1:1. Se desaconseja la amiodarona por su alta tasa de efectos secundarios que obligan a retirar el tratamiento a mediano y largo plazo.
2. En presencia de infarto antiguo, insuficiencia cardiaca o disfunción ventricular izquierda están contraindicados los fármacos antiarrítmicos del grupo IC (flecainida y propafenona), y el fármaco de elección es la amiodarona.
3. El sotalol puede emplearse en pacientes con FA sin cardiopatía orgánica, o la asociada a hipertensión arterial sin hipertrofia ventricular izquierda (HVI) o a cardiopatía isquémica sin infarto previo y con función ventricular conservada. El tratamiento se debe iniciar en el hospital, monitorizándolo, al menos, tres días, por el riesgo de producir un QT largo y arritmias letales secundarias, especialmente en pacientes con hipertrofia ventricular izquierda y mujeres.
Criterios de Ingreso hospitalario.
• Complicaciones de FA, como angina grave, insuficiencia cardiaca o tromboembolia arterial.
• Falta de control de la repuesta ventricular o de una sintomatología limitativa o potencialmente grave, a pesar del tratamiento.
• Inestabilidad hemodinámica: realización inmediata de cardioversión sincronizada en el Sistema de Urgencia Hospitalario (SUH) y, posteriormente, ingreso hospitalario.
• Inicio de regímenes terapéuticos con riesgo pro arrítmico por cualquiera de las siguientes razones: fármacos concretos, factores de riesgo cardiacos (insuficiencia cardiaca, cardiopatía isquémica, PR corto basal, historia de arritmias ventriculares) o extra cardiacos (insuficiencia renal, alteraciones hidroelectrolíticas, adición de fármacos arritmogénicos).
• Conversión de la FA a un flúter auricular tipo IC como consecuencia del tratamiento farmacológico para restaurar el ritmo sinusal.
Criterios de alta del servicio hospitalario.
Todo paciente con FA precisa una evaluación cardiológica en la que se complete el diagnóstico, se controle a largo plazo el tratamiento antiarrítmico y antitrombótico y posibles alternativas terapéuticas no farmacológicas. Por este motivo, tras el alta de los servicios de urgencia hospitalaria los pacientes deberán ser remitidos a una consulta de cardiología.
Es importante reseñar en el informe de alta del SUH los controles y vigilancia periódicos que el paciente debe recibir, como el de la frecuencia cardiaca, el nivel de anticoagulación, la función tiroidea o los electrolitos sanguíneos, así como los escalones asistenciales en que deberán realizarse, ya sea con el médico de atención primaria, en los servicios de Medicina Interna, Geriatría, o en la consulta de Cardiología (arritmias).
Ante circunstancias clínicas precipitantes resueltas o poco relevantes y restauración espontánea del RS puede admitirse el paciente en otro servicio (sala convencional de Cardiología, Medicina Interna).
Cardioversión de la FA asociada a situaciones especiales.
FA de causa aguda:
• No se debe realizar la cardioversión hasta que se corrija la causa precipitante (insuficiencia cardiaca, pericarditis aguda, insuficiencia respiratoria, sepsis, etc.). La medida terapéutica inicial se debe centrar en el control de la frecuencia ventricular y la anticoagulación si persiste más de 48 horas y no hay contraindicación.
• En el caso de FA secundaria a hipertiroidismo no se debe realizar la cardioversión hasta que transcurran más de tres meses desde que se alcanza la situación eutiroidea.
• El 95 % la FA en el postoperatorio de cirugía torácica, se auto limita tras controlar la respuesta ventricular. Por lo tanto, sólo se acude a la cardioversión antes de 48 horas si hay contraindicación formal para la anticoagulación.
• La FA en el IMA: CVE en pacientes con compromiso hemodinámico o isquemia incontrolable. Amiodarona intravenosqa en ausencia de compromiso hemodinámico. Digoxina intravenosa para control de la frecuencia ventricular, o beta-bloqueadores intravenosos en ausencia de disfunción ventricular u otras contraindicaciones.
• La FA en el Síndrome de WPW: el tratamiento de elección es la CVE, en ausencia de repercusión hemodinámica pueden utilizarse fármacos de clase IA intravenosos, como la procainamida 100 mg cada 5 minutos hasta una dosis total de 1 gr, o que aparezcan efectos adversos (hipotensión, ensanchamiento del QRS > del 50 % del basal), o clase IC, flecainida o propafenona a 2 mg/kg de peso.
• La FA en la embarazada: el tratamiento no difiere del que debe efectuarse fuera de la gestación, con excepción del tratamiento anticoagulante que requiere una evaluación especial, así como el uso de fármacos con efectos teratogénicos como la amiodarona.
FA persistente:
Cuando la FA persistente es el motivo de consulta sin haber sido diagnosticada previamente, se siguen los pasos anteriores teniendo en cuenta que la cardioversión debe ser electiva con anticoagulación previa (3 semanas antes y 4 semanas después de la fecha de la cardioversión).
Control de la respuesta ventricular.
Fármacos recomendados: Digoxina, beta-bloqueador (atenolol, propanolol, metropolol) y antagonistas del calcio (diltiazem y verapamilo). La amiodarona, aunque tiene efecto cronotrópico negativo, no está recomendada en este apartado por no reportar ventajas respecto a estos grupos terapéuticos, y presentar en cambio una alta tasa de efectos secundarios, aunque puede ser útil para mejorar la efectividad de la CVE en caso de que esté indicada.
Elección individualizada del fármaco:
• Pacientes con insuficiencia cardiaca descompensada: Digoxina sola o asociada a diltiazem. Evitar los beta-bloqueadores y el Verapamilo mientras no se restablece la clínica de insuficiencia cardiaca descompensada.
• Pacientes con disfunción ventricular sin insuficiencia cardiaca descompensada: Beta-bloqueadores solos o asociados a digoxina, iniciando el tratamiento en el hospital.
• Otras situaciones clínicas: Beta-bloqueadores o antagonistas del calcio, o combinación de estos con la digoxina.
Evaluación del grado de control de la respuesta ventricular:
Se define como frecuencia cardiaca controlada la que se mantiene entre 60 y 80 latidos por minuto en reposo, 90 a 115 por minutos durante el esfuerzo moderado, y que en la prueba de esfuerzo alcanza, durante el esfuerzo máximo, el 20 % de la frecuencia cardiaca máxima teórica.
Nivel de anticoagulación óptimo si se planifica cardioversión electiva:
Warfarina mediante vía oral hasta lograr un coeficiente internacional normalizado (INR) entre 2-3, durante tres semanas antes y tres semanas después de la cardioversión.
Manejo en sala convencional de Cardiología:
• Completar la evaluación del paciente.
Si se ha obtenido RS evaluar la necesidad de tratamiento antiarrítmico profiláctico basado en: riesgo de recurrencias, riesgo potencial de las drogas I-A, I-C (flecainida VO 100-200 mg/12 horas; propafenona vía oral 150-300 mg/8 horas) y III (amiodarona vía oral (de preferencia si ICC): impregnación con 800-1600 mg fraccionado por 7-14 días. Dosis de mantenimiento 200-400 mg; sotalol vía oral 80-160 mg/12 horas (precaución si IRC).
FA crónica:
Aceptar la arritmia y control adecuado de la frecuencia ventricular (<80 L/minuto en reposo y < de 110 L/minuto en el ejercicio).
Conducta farmacológica:
• Digital.
• Digital y bloqueadores beta-adrenérgicos.
• Digital y anticálcicos no dihidropiridínicos.
• No usar la amiodarona con la finalidad de controlar la respuesta ventricular.
• Casos refractarios: Ablación con radiofrecuencia de la unión AV e implantación de un marcapaso ventricular de demanda.
Anticoagulación a largo plazo, en caso de ser aceptada la arritmia, basado en el riesgo de embolia.
Factores de riesgo y recomendaciones para la prevención de la tromboembolia arterial en la FA permanente:
Factores de riesgo (FR) elevado:
• Accidente isquémico transitorio /Ictus isquémico o embolia arterial periférica.
• Hipertensión arterial (HTA).
• Valvulopatía mitral.
• Insuficiencia cardiaca sistólica o fracción de eyección del ventrículo izquierdo < 40 %.
• Edad > 75 años.
FR moderado
• Diabetes mellitus.
• Cardiopatía isquémica
• Edad > 65 años
Recomendaciones terapéuticas:
• Anticoagulación: (warfarina) ³ 1 FR elevado o ³ 2 FR moderados
• Anticoagulación o antiagregación: 1 FR moderado*
• Antiagregación: (Ácido acetil salicílico) < 65 años sin FR
* Individualizar de acuerdo con el riesgo de sangrado, posibilidades de un control adecuado y elección del paciente.
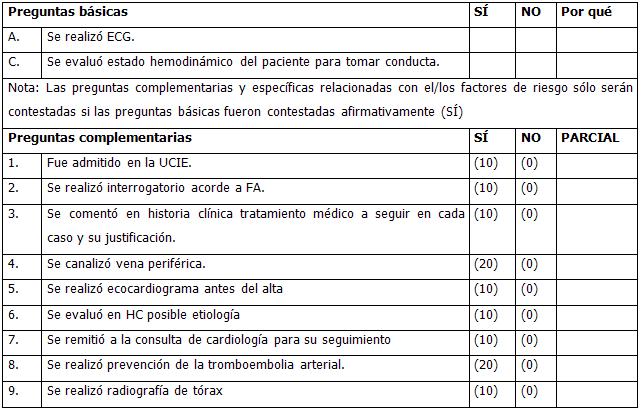
GUÍA DE EVALUACIÓN