CONCEPTOS
Muerte encefálica (ME): cese irreversible de todas las funciones intrínsicamente neurológicas del cerebro, cerebelo y del tronco del encéfalo.
La muerte encefálica implica:
• Pérdida de la respiración espontánea.
• Alteraciones del control vasomotor y cardiaco.
• Pérdida del control de la temperatura.
• Pérdida del control del balance hidroelectrolítico.
• Alteraciones de las secreciones hormonales.
Por lo tanto, los principales problemas que vamos a enfrentar en el manejo del donante potencia de órganos (DPO) son: hipotensión arterial, arritmias, trastornos hidroelectroliticos, diabetes insípida, hiperglucemia, hipotermia y trastornos de la coagulación.
Posible donante: Todo paciente con escala de coma de Glasgow ≤ 8 y en el cual no existan contraindicaciones para trasplante.
Donante potencial: Todo posible donante al cual se le realiza el diagnóstico de ME. Desde este momento y hasta que el donante sea real, se deben realizar una serie de pruebas, encaminadas a evitar la transmisión de enfermedades y a valorar y mantener los órganos a trasplantar. Esto hace que solo sean aceptados como donantes reales entre un 50 – 60% de los donantes potenciales.
Donante real: Todo paciente con ME al cual se le logra la extracción de órganos.
Donante efectivo: persona fallecida o viva que se le extrae al menos un órgano sólido o parte de él, con el propósito de trasplantarlo.
Muerte cardiaca: Muerte debido al cese irreversible de la función circulatoria y respiratoria. Un individuo que es declarado muerto bajo estos conceptos puede donar órganos y tejidos para transplante (donante a corazón parado).
Causas mas frecuente que pueden llevar al estado de ME y DPO
• Accidentes vasculares encefálicos. 45 – 50 %.
• Traumatismos craneoencefálicos severos 35 – 40 %.
• Encefalopatía anóxica 10 - 13 %.
• Tumores primitivos del sistema nervioso central 2 4 %.
Donante ideal.
Aquellos a los que se les pueden extraer los órganos y que más calidad brindan al trasplante en cuanto a funcionalidad pos implante.
Criterios generales
• Ausencia de enfermedades transmisibles (hepatitis, SIDA).
• Ausencia de enfermedad maligna (excepto tumores primarios del SNC.
• Historia médica y social aceptable (no conducta de riesgo, ni problemas médicos sistémicos serios).
• No hipotensión o dependencia de altas dosis de aminas (dopamina > 12 mcg/kg/min, o aminas múltiples).
Órganos óptimos
Son aquellos órganos procedentes de pacientes donantes ideales.
Para la admisión o exclusión de los posibles donantes de órganos se han elaborados criterios que pueden dividirse en absolutos y relativos.
Contraindicaciones absolutas
• Infección bacteriana sistémica activa, en la que tras la identificación del germen y ser tratado con el antibiótico adecuado no se obtiene respuesta.
• Infección tuberculosa incompletamente tratada.
• Infección vírica activa, incluyendo las hepatitis A,B, C, citomegalovirus, herpes simple al igual que la seropositividad de los Ac HIV.
• La positividad de las serologías frente a los marcadores de las hepatitis B y C no es actualmente una contraindicación absoluta ya que los órganos de los donantes positivos pueden ser trasplantados a receptores positivos. De la misma forma que la seropositividad para citomegalovirus, virus de Epstein Barr, herpes simple y toxoplasma, no contraindican la donación ya que es posible tratar profilácticamente a los receptores seronegativos evitando su infección.
• Enfermedad tumoral maligna (salvo ciertos tumores primitivos del SNC, carcinoma basocelular de piel y carcinoma in situ de cuello de útero.
• Adicción a drogas u otros factores de riesgo de transmisión del VIH (homosexuales, reclusos, hemofílicos, etc).
• Fallo multiorgánico.
• Enfermedad sistémica con repercusión sobre los órganos y tejidos a trasplantar (colagenosis, vasculitis).
• Enfermedad vascular ateroesclerótica avanzada.
Contraindicaciones relativas.
• Edad superior a 75 años.
• Hipertensión arterial, en especial la severa y la maligna contraindican la donación.
• Diabetes Mellitus.
• Farmacodependencia o abuso prolongado de psicofármacos (fenotiacinas, triciclicos, litio).
• Abuso de fármacos tipo analgésico, antipirético (aspirina, acetaminofén, fenotiacinas, etc.).
• Alcoholismo crónico con afectación de hígado, corazón y páncreas.
• Anemia drepanocítica y otras hemoglobinopatías.
• Enfermedades parenquimatosas o traumatismos directos de los órganos considerados para la donación
• Concomitancia de intoxicaciones exógenas con la causa que motivó la muerte encefálica.
• Pacientes en los que la muerte encefálica haya sobrevenido luego de ahogamiento, o en el curso de quemaduras.
• El comportamiento hemodinámico inestable las 24 – 48 horas previas y el antecedente de una parada cardiaca con maniobras de reanimación prolongadas.
Criterios específicos de exclusión para la extracción de riñón.
• Edad mayor de 65 años.
• Antecedentes de enfermedades renales.
• Historia de hipertensión arterial y/o diabetes mellitus.
• Oligoanuria establecida de más de 30 minutos de duración.
• Creatinina plasmática mayor 200 mmol/L.
• Presencia de malformaciones vasculares.
• Inadecuada perfusión renal.
Criterios específicos de exclusión para la extracción de hígado.
• Edad mayor de 65 años.
• Alcoholismo.
• Historia de enfermedades hepáticas.
• Tiempo de protrombina elevado.
• Determinaciones bioquímicas elevadas.
• Inadecuada perfusión hepática.
Criterios específicos de exclusión para la extracción de corazón.
• Edad mayor de 60 años antecedentes de cardiomiopatías.
• Enfermedades vasculares.
• Enfermedades congénitas.
• Enfermedades valvulares.
• Hipertensión arterial de larga evolución.
• Masaje cardíaco prolongado.
• Anomalías radiológicas, electrocardiográficas, y(o ecocardiográficas.
• Aumento de la fracción cardíaca de creatinina fosfoquinasa.
• Altas dosis de fármacos inotrópicos.
• Traumatismos torácicos.
• Alteraciones del tamaño donante-receptor.
Criterios específicos de exclusión para la extracción de pulmón.
• Edad mayor de 45 años.
• Pa O2/ FiO2 > 450 mm Hg con presión positiva al final de la espiración (PEEP) < 5 cm de H2O
• Pacientes fumadores.
• Secreciones bronquiales purulentas.
• Historia de enfermedades pulmonares.
• Anomalías en la radiografía de tórax.
• Anomalías en la fibrobroncoscopía.
• Edema pulmonar.
• Alteraciones del tamaño donante-receptor.
Criterios específicos de exclusión para la extracción de páncreas.
• Edad mayor de 55 años.
• Antecedentes de pancreatitis.
• Antecedentes de diabetes mellitus.
• Si hay elevación de la glicemia la hemoglobina glicosilada debe ser normal.
Si hay amilasemia de más de tres veces el valor normal las isoenzimas deben ser medidas y descartarse el órgano cuando la fracción pancreática está elevada.
Consideraciones del donante:
• Confirmar que se ha producido la muerte cerebral según criterios.
• Buscar criterios de exclusión para la donación de órganos antes mencionados.
• Si no se cumplen los criterios de exclusión, proponer la donación a la familia y explicar este concepto.
• Es preferible que se encargue esta tarea a representantes profesionales de algún organismo idóneo.
• Cumplir los requisitos de las normas institucionales y las leyes locales.
• Brindar apoyo emocional a la familia, cualquiera que sea su decisión.
• Si la familia acepta, el equipo de rescate de órganos supervisará los siguientes procesos: consentimiento (aceptación), realizar métodos para detectar enfermedades transmisibles y la atención médica avanzada para conservar la vida y optimizar la viabilidad de los órganos y sistemas antes de extraerlos.
Valoración clínica del donante
Está basada en protocolos encaminados a determinar la viabilidad de los órganos y asegurar que no haya riesgo para los receptores. Las características a definir están en constante evolución debido a que los criterios de aceptación de donantes se van ampliando, tanto por la experiencia que adquieren los equipos de donantes como por la presión que impone la escasez de órganos. Por tanto, los protocolos deben ser flexibles y variables dependiendo de esta evolución.
La no-viabilidad de uno o varios órganos no invalida al resto de los órganos y tejidos. Existen algunos criterios de exclusión, a los que nos referiremos a continuación:
• Valoración clínica del donante.
• Establecimiento de forma clara y precisa de la causa de muerte.
• Revisión completa de la historia clínica, valorando:
• Contraindicaciones absolutas.
• Contraindicaciones relativas.
• Hábitos personales.
• Perfusión y oxigenación tisular.
• Determinaciones analíticas y pruebas complementarias pre-extracción.
Tratamiento intensivo del DPO
Monitorización del DPO
• Monitoreo electrocardiográfico continuo (ritmo y frecuencia)
• Presión arterial invasiva de elección (sistólica, diastólica, y media), como alternativa el método no invasivo.
• Presión venosa central (PVC).
• Presión en cuña del capilar pulmonar (PCCP): según hemodinámica.
• Saturación arterial de oxigeno (Oximetría de pulso).
• Temperatura.
• Diuresis.
Estudios complementarios (controles cada 6 horas)
• Gasometría arterial
• Ionograma (Si diuresis > 500 ml/hr : cada 2 horas )
• Hemoglobina/Hematocrito
• Glicemia
Controles diarios de:
• Hemocultivo.
• Cultivo de secreciones bronquiales
• Coagulograma
• Radiografía de tórax
• Electrocardiograma.
• Controles según criterio médico de:
• Calcio, fósforo, magnesio
• Función renal
• Función hepática
Estudios para decidir inclusión como DPO
• Estudio para detección de SIDA, hepatitis C, sífilis entre otros (VIH, AgHBs, HVC, serología VDRL)
• Creatinina, Cituria, Proteinuria de 24 horas
• Ultrasonografia abdominal
• Ecocardiografía
Objetivos a conseguir en el mantenimiento del DPO
• Frecuencia cardiaca ≤ 100 mmHg
• Presión arterial sistólica (PAS) ≥ 100 mmHg
• PVC 10 – 12 mmHg
• PCCP 10 – 12 mmHg
• Diuresis > 1 mL/Kg/hr.
• Temperatura > 35 grados centígrados
• Hemoglobina ≥ 10 g/l
• Gasometría arterial ph 7.35 – 7.45, PCO2 35 – 45 mmHg, PO2 ≥ 100 mmHg
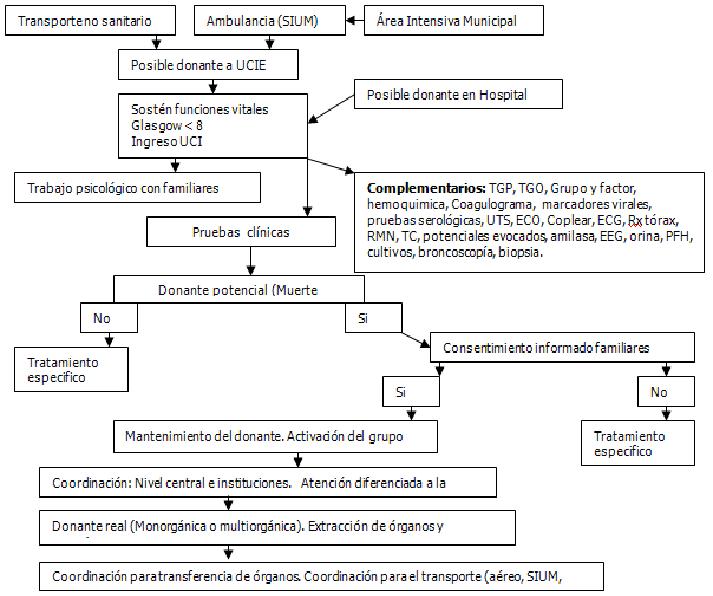
Para cumplimentar estos objetivos se realizara un abordaje por problemas
Hipertensión arterial: El uso de B bloqueadores; de elección los de corta duración (Esmolol) permiten mitigar la respuesta hipertensiva y arritmogénica durante la herniación cerebral.
Hipotensión arterial. Se sigue el siguiente esquema, las drogas incluye el uso de dopamina que puede aumentarse, si con dosis máxima no se logra PAS cercana a los 90 mmHg se pasa a norepinefrina 0.1 mcg/kg/min y se mantiene la dopamina a 3 mcg/kg/min.
Considerar dobutamina (5 – 15 mcg / kg / min ) si: insuficiencia respiratoria aguda, contusion miocardica o fallo cardiaco.

Arritmias: Considere aporte de electrolitos
Conducta ventilatoria.
Suprimir la hiperventilación terapéutica, normalizando la PCO2 (35 – 45 mmHg), para mantener el Ph normal.
En caso de hipotermia (temperatura < 34 grados) reducir la PCO2 para aumentar el Ph 0.015 unidades por cada grado de temperatura por debajo de 37 grados. Un ligero grado de alcalosis reduce significativamente el umbral de fibrilación ventricular.
Mantener la PO2 por encima de 100 mmHg con la FiO2 y PEEP más baja posible.
La Saturación arterial de O2 ha de ser mantenida en un nivel igual o superior al 90 %
El edema pulmonar neurogénico aparece con frecuencia en los donantes menores de 30 anos. Es aconsejable monitorizar la PCCP para optimizar la volemia y utilizar la PEEP menor para lograr PO2 > 100 mmHg.
Trastornos electrolíticos
Determinar regularmente Na, K, Ca, Mg y P
La hipopotasemia muy severa se puede reponer perfundiendo hasta 1 meq de potasio por minuto con control electrocardiográfico.
El resto de los desequilibrios requieren del tratamiento específico habitual.
Coagulopatía
La liberación de grandes cantidades de agentes fibrinoliticos tisulares desde el cerebro isquémico o necrótico es causa frecuente de coagulación intravascular diseminada en el DPO. Su manejo incluye:
Concentrado de hematíes, hasta llevar la hemoglobina a 10 g/l
Concentrado de plaquetas: 1 U por cada 10 kg de peso, si plaquetas < 20 x 109/L o si < 50 x 109/L y presencia de sangramientos
Plasma fresco congelado: 15 ml x kg de peso, con el objetivo de mantener tiempo de protrombina = 1.5 ratio, TPT-Caolín normal, Fibrinógeno = 100 mgL, y AT III = 80 %.
Sí las plaquetas previo a la extracción: por debajo de 50 x 10 9/L, pedir concentrados de plaquetas para el proceder.
Se deben enviar siempre 4 unidades de glóbulos al quirófano para la extracción.
Terapia hormonal
Aunque posiblemente no relacionada en su totalidad al cese del flujo sanguíneo cerebral, y a la muerte encefálica; pues se han encontrado similares alteraciones en enfermos neurocriticos sin haber llegado a la ME; es evidente que existe en el DPO una desregulación endocrina, que en un grupo no despreciable de estudios, ha estado relacionada con un deterioro de la función cardiovascular, y por consiguiente con inestabilidad hemodinámica en el DPO. Si tenemos en cuenta que la escasez de órganos para trasplantes es la principal limitante para esta alternativa terapéutica, y que de un adecuado mantenimiento del DPO dependerá en gran medida, la función inicial del injerto; y a su vez que existen estudios que han logrado demostrar que al usar un protocolo de sustitución hormonal han facilitado el mantenimiento del DPO, aumentando el pool de donantes, y de órganos a trasplantar, así como una función inicial adecuada, consideramos que ante un DPO con inestabilidad hemodinámica debe ser utilizado un protocolo de reemplazo hormonal.
En este caso consideramos adecuado ante la presencia de diabetes insípida, utilizar análogos de la vasopresina: Desmopresina; y ante un DPO con inestabilidad hemodinámica después de haber corregido con fluidos, y dosis de hasta 12 mcg/kg/min de dopamina, comenzar un tratamiento con triiodotironina 4 mcg en bolo, y continuar con infusión de 3 mcg/hr, metilprednisolona 15 mg/Kg en bolo, e insulina simple 1 unidad por hora, a lograr glucemias entre 120 y 180 mg/dl.
Poliuria y diabetes insípida
Poliuria hipotónica, con diuresis de más de 4 ml/kg/hr y densidad inferior a 1005
Hipernatremia con Na superior 145 meq/lí
Osmolaridad plasmática > 300 mosm/l
Osmolaridad urinaria < 300 mosm/l
Tener presente que el tratamiento para el edema (manitol y furosemida) puede crear poliuria con orinas hipodensas que recuerdan la diabetes insípida
Desmopresina:
0.5 – 2 mcg via ev cada 8 o 12 horas
Gotas nasales: 10 –20 mcg ( 0.1 – 0.2 ml ) cada 8 o 12 horas
Aerosol nasal: 10 mcg por cada nebulización
Hiperglicemia
Controles seriados de glicemia y electrolitos
Mantener glicemias entre 7.8 – 11.1 mmol/l
Insulina en perfusión continua, iniciando a un ritmo de 0.1 UI/ kg/hr.
Hipotermia
Elevación de la temperatura ambiente a 24 grados
Manta térmica, bolsas de agua caliente
Infusión intravenosa de fluidos calientes
Ventilación con gases húmedos y calientes
Uso de antibióticos
Se administraran específicamente ante una infección documentada, o empíricamente ante la sospecha de infección; evitando la utilización de nefrotóxicos y/o hepatotóxicos.
Consideraciones en el donante para trasplante pulmonar
• Utilización de FiO2 inferior al 50 %
• Aplicación rutinaria de 5 cm H2O de PEEP
• Evitar sobrecarga de líquidos con estrecha monitorización de PVC (entre 5 – 10 cm H2O) y PCCP.
• Evitar presiones pico mayor de 30 cm H2O
• Máximo control aséptico de la vía aérea.
Mantenimiento de las corneas
El mantenimiento cornial óptimo precisa de la oclusión ocular correcta, los párpados deben permanecer cerrados y con aplicaciones de apósitos fríos para minimizar las alteraciones corneales epiteliales. Se deben realizar instilaciones de colirios o soluciones lubricantes (lágrimas artificiales) y en ocasiones de colirios antibióticos (tobramicina o gentamicina).
El mantenimiento y el manejo correcto del cadáver DPO implica el diagnóstico precoz del estado de muerte encefálica, la evaluación rápida del cadáver como donante, el correcto mantenimiento del estado fisiológico del cadáver y la agilidad requerida en la organización y el proceso de extracción de órganos.
No deberíamos olvidar que un correcto mantenimiento del DPO tanto el médico responsable del enfermo, la enfermera y especialmente el coordinador de trasplantes deben prestar un adecuado soporte emocional a las familias que en uno de los momentos más difíciles de la vida, acceden a la donación
Medidas intraoperatorias.
• Administrar líquidos a un ritmo de 100 mL/min (frasco a frasco).
• Mantener dosis de aminas si es preciso.
• Corregir hipotermia.
• Administrar diuréticos.
• Uso de relajantes musculares, se recomienda bromuro de pancurónio a 0.1 mg/kg.
• Desconectar respirador y cesar soporte vital cuando comience la perfusión "in situ" Casos de donación renal).
• La perfusión renal se realiza con solución collins administrando de 5000-6000 ml.
• Es importante cuantificar el tiempo de isquemia caliente y fría durante el proceder.
• Una vez extraído los riñones por la técnica operatoria mediante una incisión cifopubiana, resección de ganglios mesentéricos (6-7 ganglios para estudio inmunológicos). Disección cuidadosa de aorta y cava inferior desde el tronco celíaco hasta la bifurcación de la misma, ligadura la arteria mesentérica inferior y superior, así como el tronco celíaco. Apertura de aorta y cava por las paredes anteriores y posteriores, extracción de los mismos, se realiza la cirugía de banco antes de enviarlos al centro de referencia, para lograr mejor calidad.
Manejo familiar del donante potencial
El facultativo que forma parte del equipo que diagnostica la muerte encefálica deberá conversar con los familiares sobre las causas de muerte. Deberá emplear un lenguaje lo menos técnico para que, de forma persuasiva ofrezca seguridad en sus planteamientos y le permita convencerlos sobre la donación. Esta conversación deberá efectuarse en un marco de respeto y sensibilidad ante el dolor ajeno. La conversación debe realizarse en un lugar tranquilo y cómodo donde el profesional ocupe el centro de los familiares, no deben existir ruidos ni interrupciones. El psicólogo debe tener un importante papel estando en contacto estrecho con los familiares con el fin de brindar un apoyo psicológico y comprometer a la familia aun más con el médico y la institución.
Aunque el paciente en vida haya expresado su interés por donar sus órganos ante cualquier situación, es importante contar siempre con la decisión de familiares allegados que serian definitivamente los que consienten la donación. No deja de haber casos en que se expresa la negatividad a la donación del órgano y en tal caso ese deseo es respetado.
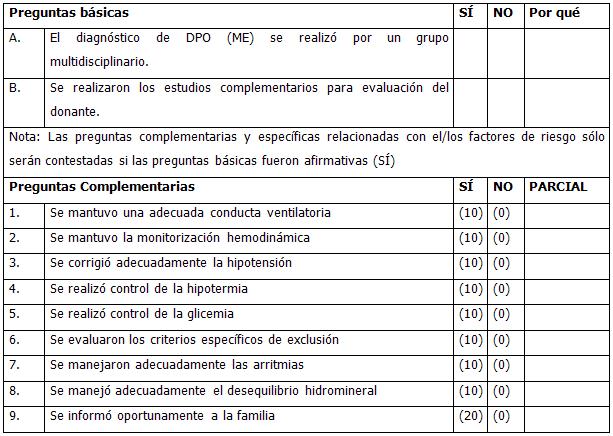
GUÍA DE EVALUACIÓN