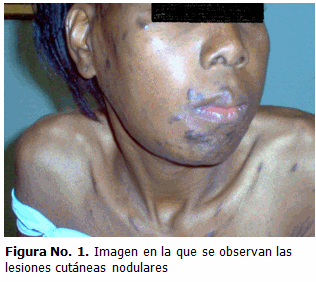
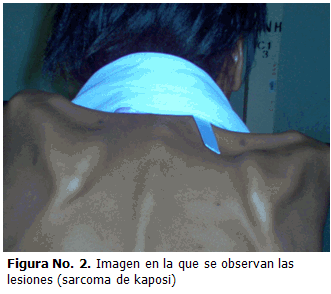
INTRODUCCIÓN
El sarcoma de Kaposi (SK) fue descrito por primera vez en 1872 en Viena por el dermatólogo húngaro Moritz Kaposi, bajo el nombre de "sarcoma múltiple pigmentado idiopático". Existen al menos cuatro formas clínicas de Sarcoma de Kaposi: clásico, endémico, iatrogénico y epidémico. (1,2)
Sarcoma de Kaposi Epidémico
En 1981, se observó por primera vez una forma fulminante y diseminada de SK en hombres jóvenes homosexuales o bisexuales que era parte de una epidemia que ahora se conoce como el Síndrome de Inmunodeficiencia Adquirida (SIDA). (1,2)
El SK es la neoplasia más frecuentemente asociada al virus de la inmunodeficiencia humana (VIH) y al SIDA, durante la década de los años 1980, fue encontrado en casi el 40% de los pacientes masculinos que sufrían de SIDA en los Estados Unidos de América, con especial predilección por hombres homosexuales. (1,3)
Sin embargo, en África donde la vía de transmisión heterosexual es la más importante, puede ser encontrado también en niños y mujeres. (3,4) Desde el descubrimiento del VIH en África, la incidencia del SK se incrementa en países donde antes era relativamente raro, pero donde la prevalencia del herpes virus humano 8 (HHV-8 por sus siglas en Inglés) y VIH es alta. (5,6)
En San Francisco la incidencia del SK durante 1987-1991 fue de 32 por cada 100 000 personas, para 1998 la incidencia había disminuido a 2.8 por cada 100 000, reducción debida en gran medida a la introducción de terapias antiretrovirales altamente efectivas (TARV). (3)
Tarde o temprano, en la mayoría de los pacientes con SK epidémico se disemina la enfermedad, este generalmente evoluciona de manera ordenada, de unas pocas lesiones muco-cutáneas localizadas o generalizadas a una enfermedad cutánea con lesiones más numerosas y generalizada con complicación de ganglios linfáticos, el sistema gastrointestinal y otros órganos, el promedio de vida en SK-SIDA es de 15-24 meses. (1-4,6)
El SK pleuro-pulmonar es un signo ominoso que ocurre generalmente al final del curso de la enfermedad. La afectación pulmonar sin lesiones cutánea puede presentarse en un 15-20% de los pacientes. (7) La mayoría de los pacientes con SK epidémico mueren de complicación con una o más infecciones oportunistas.
Una clave importante para descifrar el enigma de la patogénesis del SK fue el descubrimiento en 1994 por Chang y colaboradores de un virus herpes gamma en lesiones cutáneas de pacientes con SK y el HHV-8, conocido también como virus herpes del sarcoma de Kaposi (KSHV por sus siglas en Ingles). (2, 4,6).
El HHV-8 fue identificado en las biopsias de tejido de los sarcomas de casi todos los pacientes que padecen de SK clásico, africano, relacionado con un trasplante o asociado con el SIDA, pero no fue hallado en tejidos no afectados.
Martín y colaboradores demostraron que en pacientes infectados con el VIH y HHV-8 la probabilidad de desarrollar un SK en 10 años es casi de un 50%.(3)
La incidencia del SK varía considerablemente entre pacientes VIH positivos según los grupos de edades, alcanzando 21-40% entre adultos homosexuales o bisexuales, en tanto que en la población pediátrica y hemofílicos sólo son de 1.6 y 1 % respectivamente. (8) En otros grupos de pacientes infectados por VIH es muy baja, y se distribuye de la siguiente manera: 3% en pacientes adictos a drogas intravenosas, 3% en pacientes con transfusión sanguínea y 3% en mujeres con SIDA. De los pocos casos reportados de mujeres con SK-SIDA, se sabe que sostenían relaciones sexuales con hombres bisexuales; hasta ahora no se han informado casos en mujeres que adquirieron la infección a través del contacto exclusivamente heterosexual o por transfusión sanguínea. (9) Entre la población autóctona africana las prácticas homosexuales o bisexuales son extremadamente infrecuentes.
En la distribución por sexo de las personas afectadas por este sarcoma, se evidencia una gran diferencia en los casos de SK endémico africano, cuya frecuencia es igual en hombres y en mujeres, mientras que, en los casos de SK-SIDA hay un claro predominio en hombres, específicamente en el grupo de homosexuales, con una relación hombre a mujer de 8:1. (9)
No existen pruebas concluyentes de que la prevalencia de HHV-8 haya cambiado en África desde la propagación del VIH. De hecho el HHV-8, un ganma 2 herpesvirus, se cree que haya coexistido junto con el Homo sapiens desde su origen. Otro estudio realizado en África demostró que los anticuerpos anti-HHV-8 estaban presentes antes del surgimiento de la epidemia del VIH a niveles similares a los reportados en la actualidad. El HHV-8 es igualmente prevalente en hombres como en mujeres en África y el SK sigue siendo mucho más frecuente entre los hombres. (5)
En la actualidad un gran número de galenos cubanos se encuentran cumpliendo misión internacionalista en diversos países del continente africano, Asia y América Latina donde la incidencia del VIH es muy alta y este tipo de tumor es frecuente, y fácil de reconocer. Se ha observado que muchos pacientes responden adecuadamente a los tratamientos antiretrovirales, es por todo lo anterior que consideramos importante el tema.
Se decide publicar el caso para contribuir con la educación de jóvenes médicos, compartir experiencias y difundir las características clínicas de este tumor con las modalidades terapéuticas más frecuentemente utilizadas.
PRESENTACIÓN DEL CASO
Paciente femenina de la raza negra, de 27 años de edad, que ingresó en nuestro servicio porque 2 meses atrás notó lesiones nodulares de color púrpura en la cara, parte superior del tórax y extremidades, presentó cansancio fácil y falta de aire, que se acentuaba con ejercicios físico, anorexia, pérdida de peso y tos productiva; antecedentes patológicos personales, tuberculosis pulmonar en 1999 (finalizó tratamiento). VIH positiva desde 2006, recibió drogas antirretrovirales desde julio 2007, alergias ninguna; no fuma, ni toma bebidas alcohólicas; historia sicosocial soltera, estudiante y trabajadora casual. Examen físico: mucosas pálidas y húmedas.
Examen respiratorio: matidez a la percusión en la base derecha con murmullo vesicular disminuido. Frecuencia respiratoria (FR): 22 respiraciones por minutos; examen cardiovascular, pulso radial: 129 pulsaciones por minuto. Tensión arterial (TA): 100/59 mm Hg, no soplos.
Abdomen: suave depresible, no visceromegalia. Edema de fácil godet en miembros inferiores hasta tercio medio de la pierna.
Exámenes complementarios: hemograma completo, leucocitos 6.5x109/l, conteo de células rojas 2.25, Hb 6g/l, volumen corpuscular medio 89.8, hemoglobina corpuscular media 26.7, CHCM 29.7, conteo de plaquetas 165x109/l. Pruebas funcionales hepáticas: bilirrubina total 10mmol/l, proteínas totales 65g/l, albúmina 21g/l, fosfatasa alcalina 96u/l, GGT 12 u/l, transaminasa glutámico pirúvica 7 u/l, transaminasa glutámico oxalacetica 17 u/l.(13-09-2007), sodio 132 mmol/l, potasio 4.3 mmol/l, cloro 98mmol/l, urea 5.6 mmol/l, creatinina 66 mmol/l. Vitamina B12 sérica 119ng/l, ácido fólico sérico 9.1 ng/l, hierro sérico 5.8mmol/l, transferrina1.6 g/l, saturación de transferrina 14%, ferritina 96mg/l (14-09-2007). Serología para sífilis negativa. Examen de liquido pleural, conteo de células rojas 250, conteo de linfocitos 98, polimorfos nucleares 2, ADA 10.0, proteínas totales 41g/l, LDH 91u/l, citología no células anormales, escasas células mesoteliales, linfocitos y hematíes, cultivo para tuberculosis negativo. Esputo BAAR x2: negativo, cultivo de esputo para tuberculosis negativo, conteo absoluto de CD4 35, % CD 4 de linfocitos 1.48%, carga viral 18 000 copias ARN/ ml, valor logarítmico 4.26, hemograma después de ser transfundida, leucocitos 8.9, Hb 9.0 g/l, conteo de células rojas 3.21, plaquetas 187. Radiografía de tórax: confirma la presencia de un derrame pleural en la base derecha, área cardiaca dentro de límites normales.
Impresión diagnóstica: Enfermedad retroviral estadio IV según los criterios de la Organización Mundial de la Salud (OMS), SK epidémico, derrame pleural derecho, probable relacionado con el sarcoma de kaposi, sin embargo la causa tuberculosa no puede descartarse totalmente.
Tratamiento recibido Lamivudina 150 mgs cada 12 horas, estavudina 30 mgs cada 12 horas, nevirapina 200 mgs cada 12 horas, cotrimoxazol 960 mgs diariamente. Fue remitida al Servicio de oncología del Hospital Provincial de Puerto Elizabeth donde inició tratamiento con vincristina 2 mgs semanalmente. Fue egresada de nuestro servicio y mantuvo tratamiento con drogas antirretrovirales y quimioterapia, recibió 8 ciclos de vincristina con escasa respuesta, posteriormente se le añadió bleomicina y dexametasona, su evolución siguió siendo pobre, por lo que se decidió introducir doxorubicina y adriamicina, hasta su lamentable fallecimiento.
DISCUSIÓN
Desde hace más de veinte años se ha pensado que algún virus estaba implicado en la patogenia del SK y que este virus podría ser transmitido por vía sexual.
Son numerosos los agentes infecciosos a los que se ha intentado atribuir un papel en el desencadenamiento de las lesiones de sarcoma de kaposi: citomegalovirus, virus del papiloma humano tipo 16, virus herpes humano tipo 6, mycoplasma penetrans. (8)
El HHV-8 parece ser la condición necesaria, pero no suficiente para el desarrollo de la enfermedad, necesitando una seroconversión, que parece inducida por el déficit inmunitario que provoca la infección por el VIH y que también se produce en las formas iatrogénicas de sarcoma de Kaposi debido a los tratamientos inmunosupresores en enfermos trasplantados, remitiendo las lesiones al suspender los tratamientos inmunosupresores y en los enfermos de SIDA al mejorar su inmunidad con los tratamientos antirretrovirales.(6,8)
Este virus produciría una interleuquina (IL) similar a la IL humana 6, que induce crecimiento endotelial vascular.
Por otro lado existen estudios que vinculan el desarrollo de lesiones de SK no sólo al déficit inmunitario, sino que plantean una colaboración del HHV-8 con el virus de la inmunodeficiencia humana, siendo este un colaborador necesario, a través de su proteína Tat para el desarrollo de las lesiones de Kaposi.(6,8)
Un tema distinto seria el método de transmisión del HHV-8, que la mayoría de autores plantean por vía de transmisión sexual, fundamentalmente prácticas homosexuales entre varones, no encontrándose partículas virales en algunas poblaciones heterosexuales, aunque en algunos estudios se ha demostrado transmisión vertical madre-hijo y también puede ser transmitido a través de trasplante de órganos.(8)
Se puede dividir en tres grupos principales. Clasificación:
a) Según la epidemiología:
- Esporádico.
- Endémico (africano)
- Epidémico (SIDA)
- Iatrogénico (pacientes trasplantados, tratamiento inmunosupresor).
b) Según la clínica:
Localizado (piel).
- Temprano
- Agresivo
- Nodular
Generalizado.
- Linfadenopático
- Sistémico
c) Histología:
Se clasifica en temprano o de inicio, fase nodular o tumoral, que será: angiomatoso, fusocelular, inflamatorio, patrón mixto, pleomórfico.
Las formas tempranas o "patchy" son particularmente frecuentes en pacientes con SIDA. En la era "pre SIDA" se describían 4 estadíos o tipos clínicos que eran: nodular cutáneo, agresivo cutáneo, linfadenopático y sistémico. (2, 4,7.8)
En la era del SIDA se agrega la forma temprana o "patchy", en la que la lesión es dérmica, superficial, pudiendo tener afectación orofaríngea y en la submucosa del tubo digestivo. Se trata de maculo-pápulas violáceas que, desde el punto de vista histológico, corresponden a acumulo de vasos con atipias leves. (7)
En la fase nodular se reconocen tumoraciones de tamaño variable, desde pocos milímetros (mm) hasta tres centímetros (cm), que son de topografía dérmica, pero que rápidamente se ulceran y pueden acompañarse de edema.
La forma agresiva puede ser exofítica o infiltrante (esta última erosiona el hueso). (7) En la forma linfadenopática la evolución es fatal, con muerte de los pacientes en menos de 1 año, se ve en 25 a 50% de los SK en niños africanos. (4) Con poli-quimioterapia (PQT) se logran períodos largos de remisión. La forma sistémica es también rápidamente progresiva, con muerte en pocas semanas. Se asocia a inmunodepresión iatrogénica o al SIDA con disminución y disfunción severa de los linfocitos T.
Las diferentes formas clínico-epidemiológicas presentan el mismo aspecto histológico, tanto en piel como en otros órganos. (7,10) Al inicio siguen el trayecto de los vasos, bronquio, apéndices cutáneos, áreas portales, para, desde allí crecer hacia el parénquima. A medida que progresa la enfermedad, el sarcoma de Kaposi esta integrado básicamente por tres elementos que son: vasos, células inflamatorias y células fusiformes. De acuerdo al predominio de uno u otro de estos elementos, se denominará al tumor: angiomatoso, inflamatorio o fusocelular. También se reconocen de forma característica, glóbulos hialinos o eosinófilos. (7,10)
Características clínicas
Clínicamente se caracteriza por la aparición de manchas, placas o nódulos violáceos, rojas, rosadas o marrones, de diferentes tamaños pudiendo oscilar desde varios mm hasta varios cm, las lesiones cutáneas son generalmente palpables y no pruriginosas, cuando afectan la planta de los pies pueden ser dolorosas y afectar la marcha.(10-12)
En la piel las lesiones del sarcoma de kaposi se encuentran típicamente en la mitad superior del cuerpo: cara (particularmente la nariz), parte alta del tórax, genitales y miembros inferiores, aunque pueden presentarse en cualquier parte del cuerpo. (13)
Existen formas de presentación ganglionar sin lesiones de la piel o como lesiones de las mucosas de la boca e intestino. Es frecuente la afectación de la mucosa bucal, sobre todo del paladar y encías. La presencia de edema o ulceración, afectación extensa de mucosa oral y la afectación visceral distinta de la ganglionar son considerada como factores de mal pronóstico.
La afectación visceral es frecuente; en la mitad de los pacientes con lesiones de la piel se detecta afectación visceral, sobre todo a nivel intestinal, aunque también se puede producir afectación de hígado, pulmón, ganglios linfáticos, cerebro y corazón.
Manifestaciones del aparato digestivo
La afectación gastrointestinal es encontrada en el 40% de los pacientes con SK y puede llegar hasta un 80% en hallazgos necrópsicos, las manifestaciones del aparato digestivo pueden presentarse si lesiones cutáneas. La afectación a este nivel puede causar dolor abdominal, pérdida de peso, nausea, vómitos. El examen de sangre oculta en heces fecales constituye un recurso de gran valor en el pesquisaje de estas lesiones. La afectación de la mucosa oral puede causar problemas para la deglución de alimentos y el habla, en el estómago o los intestinos pueden ser fatales, causando sangramientos y obstrucción de los órganos afectados.
Otra manifestación gastrointestinal es mayormente debida a la infiltración de la vesícula y el árbol biliar produciendo manifestaciones clínicas de ictero obstructivo similares a las observadas en la Colangitis esclerosante. (11)
Sistema respiratorio
La afectación pulmonar suele ser rápidamente fatal, simulando una neumonía por Pneumocystis Jirovecii; los síntomas más frecuentes son: disnea, tos y menos frecuente hemoptisis. El 80% de los pacientes con manifestaciones respiratorias tienen lesiones cutáneas, el derrame pleural están presente en el 70% de los pacientes con SK pulmonar, la radiografía de tórax generalmente muestra infiltrado bilateral en los lóbulos inferiores que borra el diafragma y el borde mediastinal. (10-13) La afectación pulmonar en el SK se ha demostrado con broncoscopio de fibra óptica entre un 6-32% en los pacientes con SIDA, pudiendo alcanzar hasta un 21-49% en aquellos con síntomas respiratorios y lesiones cutáneas y en estudios post-morten entre un 47-75%. (9) El promedio de vida después del diagnóstico antes de la introducción de la terapia antirretroviral (TARV) era entre 3-10 meses. (12,13)
La tomografía axial computarizada (TAC) es un examen de gran utilidad, confirmando las lesiones pleuro-pulmonares en el 90% de los casos, la ultrasonografía puede ser utilizada en pacientes con lesiones pleurales o para realizar toracocentesis guiada. (10,14)
Si el SK afecta a los ganglios linfáticos, puede causar un edema severo de las extremidades, la cara o del escroto. En la médula ósea se reconoce su compromiso en 20% de las formas agresivas. (11)
Se estima que aproximadamente el 20% de los pacientes con SK presentaran lesiones del sistema genitourinario, el pene y escroto son los órganos más frecuentemente afectados, pero menos del 3% presentaran lesiones iniciales a este nivel. (15) En ocasiones el SK puede afectar los ojos, particularmente los párpados, conjuntiva, saco lagrimal y raramente puede ser encontrado dentro de la orbita. (16)
El diagnóstico diferencial se debe establecer con otras lesiones que presenten vasos y células fusiformes en cantidades variables tales como acroangiodermatitis (secundaria a oclusión venosa) granulomas piógenos, cicatrices, otros tumores vasculares, histiocitomas fibrosos benignos o malignos, angiomatosis bacilar y otros sarcomas.
Tratamiento
Un estudio presentado en la Quinta conferencia de Chicago sobre retrovirus e infecciones oportunistas concluyó que la respuesta del SK a la TARV no es uniforme. Así, aproximadamente dos meses después de un aumento significativo de la carga viral del VIH suele producirse un empeoramiento significativo del SK, mientras que la mejoría del SK tras una reducción de la carga viral es más variable. (4)
Puede ser posible que las TARV impidan la aparición de nuevos casos de SK, pero que su efecto sobre un SK ya establecido sea limitado. Así, la TARV tendrá un impacto claro en la incidencia de casos de SK, pero estas drogas no siempre pueden suprimir el VIH, y aún en los casos en que puedan hacerlo, no siempre logran provocar la remisión del SK. (1, 8,17)
Antivirales: Se ha demostrado que tanto foscarnet, cidofovir y el ganciclovir, antivirales utilizados actualmente en el tratamiento del citomegalovirus (CMV), reducen en alrededor del 60% el riesgo de desarrollar sarcoma de kaposi. Estas observaciones han propiciado que muchos investigadores intentaran demostrar la efectividad de fármacos antivirales contra el virus herpético del sarcoma de Kaposi. (1,8)
In vitro, muchos análogos de los nucleósidos, incluyendo no sólo foscarnet, ganciclovir, sino también cidofovir y adefovir han demostrado tener considerable actividad contra el HHV-8. Cabe señalar que los análogos de los nucleósidos sólo interfieren en la producción de nuevo ácido desoxirribonucleico (ADN) viral, pero no pueden eliminar las células crónicamente infectadas, por lo que su efecto sobre el SK establecido dependerá de sí la permanencia de la enfermedad requiere la infección continua de nuevas células, lo que es dudoso. En todo caso, al menos los fármacos antivirales podrían limitar una mayor expansión de los tumores o prevenir la enfermedad antes de que ésta aparezca. (8)
El tratamiento del sarcoma de kaposi es paliativo y depende de sí el sarcoma se localiza sólo en la piel, o si se ha diseminado a otras partes del cuerpo. (4, 8,17)
Tratamiento tópico
Para el tratamiento local de las lesiones se han empleado tradicionalmente métodos quirúrgicos, radioterapia, crioterapia con nitrógeno líquido, escleroterapia con tetradecyl-sulfato de sodio e inyecciones intralesionales de diferentes compuestos (dinitroclorobenceno, factor de necrosis tumoral, vinblastina, interferon alfa, etc.).(1, 3, 8,18,)
Alitretinoin (Panretin) 0.1%: Es el único medicamento tópico que se analizó en estudios clínicos y que está aprobado por la Administración de drogas y alimentos para el tratamiento de las lesiones cutáneas del SK. Este gel se aplica en las lesiones, tres o cuatro veces al día, y los estudios han demostrado que es efectivo. (1, 3, 4, 8,18)
Con la radioterapia la mayoría de las lesiones regresan aunque suelen recidivar en 4-6 meses; puede ser útil para las lesiones con componente cosmético, el SK genital con dificultad para la micción y en la afectación sistémica de la cavidad oral. (1, 4, 8,18)
El edema secundario a la obstrucción linfática puede beneficiarse temporalmente con la radioterapia pero en general no se recomienda para el tratamiento de la afectación visceral salvo en pacientes con expectativas de supervivencia muy limitadas. También se recomiendan para lesiones del SK que aparecen en los pies, debido a que otros tratamientos locales pueden resultar dolorosos en estas partes del cuerpo. (1, 4,8)
En la quimioterapia intralesional también es frecuente la recidiva en unos pocos meses. La crioterapia se ha utilizado para mejoría cosmética de lesiones pequeñas y planas, especialmente en la cara.
El tratamiento local presenta la ventaja de escasa o nula toxicidad sistémica y la ausencia de efectos inmunosupresores añadidos, además de su carácter usualmente circunscrito.
Tratamiento sistémico
En los últimos años se ha avanzado mucho en el conocimiento de la patogénesis viral e inmunológica del sarcoma de kaposi. Estos avances se han visto acompañados por la mejoría en el tratamiento del VIH, específicamente la utilización TARV. Todo ello ha resultado en una menor incidencia del SK en la población infectada por el VIH del mundo desarrollado. (1, 4, 8,18)
Se han empleado diferentes agentes antineoplásicos (bleomicina, vinblastina, vincristina, doxorubicina, epirubicina, etopósido, etc.) solos, combinados entre ellos o asociados a antirretrovirales.
Las terapias tradicionales sólo tienen efecto a corto plazo, eventualmente surgen nuevos tumores del sarcoma; además los efectos secundarios son considerables, especialmente en el caso de la quimioterapia (neutropenia, neuropatía periférica, toxicidad cardiaca, pérdida de cabello y náuseas) pero también con las terapias locales, que causan dolor, ulceración, irritación de la piel y alteraciones de la pigmentación cutánea.(1,4)
En general en todos los pacientes con SK se recomienda tratamiento. En los pacientes más estables inicialmente puede ser suficiente la terapia local al igual que en los pacientes que presentan escasas lesiones con alto componente cosmético; en estos casos la radioterapia puede ser una elección razonable. El interferón y su combinación con antivirales se pueden considerar en pacientes con lenta evolución del SK o ligeramente sintomáticos. (1)
La quimioterapia se debe considerar para los pacientes que presentan una rápida evolución, con afectación amenazante de la vida, afectación pulmonar o linfedema severo.
Desde 1995 la Administración de Drogas y Alimentos (FDA) ha aprobado cuatro fármacos específicamente indicados para el tratamiento del sarcoma de kaposi: la doxorubicina liposomal (Doxil) y la daunorubicina liposomal (DaunoXome), así como recientemente paclitaxel y el ácido 9-cis-retinoico o alitretinoína. (1, 8, 10,13, 16, 17)
La quimioterapia liposomal (Doxil o DaunoXome) puede ser una alternativa válida y menos tóxica que la sistémica, estos medicamentos representan un nuevo tipo de medicinas para quimioterapia estándar. Cada dosis de estos medicamentos contiene millones de esferas microscópicas de grasa, y cada esfera contiene la forma activa del medicamento. Esto aumenta la cantidad de medicamento en la sangre, lo que a su vez aumenta la cantidad de medicamento que llega a cada lesión. Algunas investigaciones revelan que la quimioterapia liposomal es más efectiva que la quimioterapia estándar. (1, 4, 8. 13)
Se puede utilizar DaunoXome 40 mg/m2 IV durante 60 minutos cada 2 semanas. (2, 10) Doxil 20 mg/m2 cada 2-3 semanas, efectos secundarios reportados neutropenia, alopecia, nauseas, falta de aire etc.
En los casos que exista una recaída después de la quimioterapia, el paclitaxel (taxol) es una alternativa a considerar. La dosis recomendada es 100 mg/m2 IV en un periodo de 3 horas cada 2 semanas o 135 mg/m2 cada 3 semanas, siendo recomendable la premedicación con dexametasona, difenhidramina y ranitidina. (8, 13)
El paclitaxel es sumamente tóxico, los efectos secundarios más comunes son leucopenia, anemia además de pérdida de cabello, debilidad, diarrea, nauseas o vómitos, dolor muscular o en las articulaciones y neuropatía periférica. (8)
Los pacientes con mielosupresión deben recibir factores estimulantes de colonias y se debe recomendar profilaxis para las principales infecciones oportunistas.
Desde principios de 1999 se están utilizando otros tratamientos, entre los que mencionaremos al interferon alfa aprobado en 1998 como terapia sistémica anti-SK en algunos pacientes. (4, 8)
Este medicamento ataca el VIH (antiviral), ayuda a mejorar la función inmunológica (inmunomodulador), acción antiproliferativa y antiangiogénica, ha demostrado ser un tratamiento efectivo contra el SK.
La investigación sobre el interferón alfa (IFN-a) se ha centrado en su combinación con antirretrovirales, sobre todo análogos de los nucleósidos y especialmente zidovudina (AZT). En 1996, un estudio de IFN-a y AZT para el tratamiento del sarcoma de kaposi describió una regresión del SK en aproximadamente el 30% de los pacientes participantes, frente a una tasa de respuesta menor del 10% con mono terapia de IFN-a.
La mayoría de los estudios de la combinación IFN-a y AZT han descrito una alta ocurrencia de neutropenia. Por ello, se ha tratado de combinar IFN-a con análogos de los nucleósidos con menos efectos supresores de la médula ósea, como didanosina (DDI), la incidencia de neutropenia parece ser muy inferior con esta segunda combinación. (4)
Él interferón alfa puede provocar efectos secundarios entre los que podemos mencionar fiebre, escalofríos, neutropenia, hepatotoxicidad, reacción anafiláctica etc. Estas reacciones adversas son menos frecuentes y hay mejor respuesta terapéutica en pacientes que tienen recuentos de células CD4 relativamente altos (más de 200 células/mm3) antes de iniciar el tratamiento. (1,4, 13) El interferón alfa se ha utilizado en dosis de 30 millones U/m2 Subcutáneo (SC) 3 veces por semanas. (2, 4)
También se ha utilizado la gonadotropina coriónica humana (HCG). (4, 19)
A pesar de la terapia con drogas antirretrovirales y quimioterapia él pronóstico de los pacientes, sigue siendo pobre y la mayoría fallece dentro de los primeros 6 meses de haber iniciado tratamiento. Contrariamente a lo reportado en la literatura mundial, donde la incidencia del sarcoma de kaposi ha bajado considerablemente desde la introducción de las terapias antirretrovirales altamente activas, en Sudáfrica un número creciente de pacientes son diagnosticados con SK, por ejemplo en el período comprendido entre 1988-1996 la incidencia del tumor se triplicó comprobándose que se puede presentar en pacientes VIH positivo de ambos sexos.