Introducción
El cáncer ocasiona millones de muertes al año y origina altos costos a los sistemas sanitarios. Los tumores primarios del Sistema Nervioso Central (SNC) corresponden al 2 % de todos los tipos de cáncer. A escala mundial en el año 2020 se diagnosticaron 308 102 casos de tumores del SNC, con 251 329 defunciones. Dentro de los tumores de encéfalo primarios, el 38 % son de alto grado de malignidad.(1) En el 2018 en Cuba, esta entidad ocasionó la muerte de 617 pacientes, con una tasa ajustada entre 5,6 y 5,4 por cada 100 000 habitantes.(2)
El tratamiento de primera línea de los tumores de alto grado es la cirugía, seguido de radioterapia, pero se ha obtenido un limitado progreso en su tratamiento.(3,4,5) Se estima que en más del 95 % de los casos ocurre una recurrencia en el área adyacente a la resección.(6,7) La sobrevida de pacientes de alto grado persistentes o recidivantes es alrededor de seis meses, y menos del 10 % sobrevive dos años.(8,9).
La aplicación de enfoques inmunoterapéuticos, especialmente estrategias de combinación, han demostrado alguna eficacia contra el glioblastoma multiforme (GM). La asociación de inhibidores del punto de control inmunitario con radioterapia parece ser una estrategia a considerar; sin embargo, las reacciones de disparidad en los estudios indican la necesidad de realizar investigaciones adicionales para evaluar la eficacia en grupos específicos de pacientes. Estas terapias dianas inducen pocas respuestas completas en los enfermos, no han sido curativas y han mostrado toxicidad, sin lograr beneficios notables en la supervivencia y su costo.
Estos resultados tan pobres conducen a la búsqueda de nuevas modalidades terapéuticas que produzcan un impacto real en la supervivencia, en condiciones de seguridad para los pacientes y con factibilidad económica en su empleo.
En este trabajo se pretende demostrar la factibilidad económica de la combinación de interferones (Heberferón®), producto nacional del Centro de Ingeniería Genética y Biotecnología, frente a otros productos aprobados o en estudio en los contextos nacional y foráneo en el tratamiento a pacientes con tumores cerebrales de alto grado de malignidad sin opciones terapéuticas.
Métodos
Se realizó un análisis económico de tipo costo-efectividad, que es una de las formas de análisis más usada en la evaluación de tecnologías sanitarias. Se utilizaron los datos clínicos generados prospecti-vamente durante una investigación realizada en el Hospital Provincial Clínico-Quirúrgico Arnaldo Milián Castro, de Villa Clara, Cuba. En ella se incluyeron pacientes con tumor cerebral recurrente o pro-gresivo de alto grado de malignidad que recibieron tratamiento con el anticuerpo monoclonal nimotuzumab o con una combinación de interferones entre los años 2009 y 2020.
Los criterios de inclusión fueron: edad ≥18 años, cualquier género y color de piel, escala de Karnofsky al inicio del tratamiento (EK) 60-100 %, criterio diagnóstico anatomo-patológico, evaluación por imá-genes, parámetros hematopoyéticos en rango normal, al menos cuatro semanas después de la cirugía y con los criterios de recuperación, las pacientes en edad fértil utilizaron un método anticonceptivo eficaz. Quedó expresada por escrito la voluntariedad del paciente.
Los criterios de exclusión fueron los siguientes: infarto de miocardio en los últimos 6 meses, angina severa o inestable, implante de bypass coronario o periférico, insuficiencia cardíaca congestiva sinto-mática, embarazo, puerperio o lactancia, infección activa, hipersensibilidad al Interferón, enfermedades crónicas descompensadas, enfermedades con compromiso metabólico, muy mal estado general, con-vulsiones intratables médicamente o trastorno psiquiátrico grave.
De los 44 pacientes con criterio diagnóstico para ser incluidos, se excluyeron cuatro enfermos ya que dos de ellos no ofrecieron su consentimiento para participar y los otros dos presentaron alguno de los criterios de exclusión. De ese modo quedó constituida una muestra de 40 pacientes. De ellos, 23 recibieron la combinación de interferones y 17 se trataron con nimotuzumab.
Se llevó a cabo una evaluación económica completa del tipo costo efectividad (CE), tomando como medida de efectividad la supervivencia global (SG) en meses de los pacientes tratados. Los resultados se expresaron bajo la relación costo efectividad media (CEM) y costo efectividad incremental (CEI). La perspectiva adoptada en el estudio fue la correspondiente a un proveedor de servicios de salud pública. El horizonte temporal para este análisis fue de 12 meses, compatible con el modelo propuesto adoptado, y consistente con el tiempo promedio de SG para estas enfermedades registrado en la literatura, por tanto, no se utilizó la tasa de descuento.
La SG se estableció a los 6, 12 meses y al cierre del estudio, se calculó del total de pacientes que recibieron tratamiento, el porcentaje de pacientes vivos a los 6, 12 meses y al fin de la investigación, a partir del diagnóstico y del inicio de tratamiento por grupo. Los comparadores empleados fueron las alternativas terapéuticas consideradas en la literatura como efectivas para esta enfermedad y el grupo de control histórico. El parámetro de efectividad para cada uno de los comparadores se obtuvo haciendo una búsqueda sistemática en Medline (Pubmed) y Cochrane, se seleccionaron las fuentes de información de efectividad teniendo en cuenta: nivel de evidencia I o II de acuerdo con el tipo de diseño, el poder, el grado de confiabilidad, el tamaño de muestra y la tasa de descontinuación, estándar equiparable de efectividad y descripción del resultado más favorable para cada fármaco. En consecuencia, con la efectividad reportada, se especifica la dosis correspondiente para cada medicamento. Se asumieron como costos el precio de compra de los medicamentos en el mundo, sin contemplar los costos por manejo de los eventos adversos de cada molécula ni los costos del paciente o de la sociedad debidos a la pérdida de productividad.
El CEM se interpretó como el costo adicional que se debe pagar para obtener una unidad del beneficio y se expresa como el cociente que se obtiene al dividir el coste neto de la intervención por su beneficio neto o efectividad. Se consideró una variable cuantitativa continua. El CEI representó el costo adicional en el que se debe incurrir para obtener una unidad adicional de efectividad entre un esquema y otro. Se presentaron como la razón entre la diferencia en el costo de dos posibles intervenciones y la diferencia en su efecto. Es decir, los costos de la mezcla de interferones menos los costos del comparador, sobre los beneficios de esta menos los beneficios del comparador. Se consideró una variable cuantitativa continua.
Se realizó una evaluación económica completa, se compararon los efectos sobre la salud y sobre los recursos de varias opciones de tratamiento. Los efectos sobre los recursos o costos se valoraron en uni-dades monetarias, y los efectos sobre la salud en unidades naturales de efectividad, supervivencia global en meses en el caso específico de este estudio. Fue condición indispensable que los efectos de los tratamientos se midieran en la misma unidad de efectividad en las diferentes alternativas. La principal ventaja de este análisis es la posibilidad de expresar los resultados en las mismas unidades usadas en investigaciones clínicas o en la práctica diaria.
Para el análisis estadístico se empleó el software SPSS (Statistical Package for Social Sciences) versión 20.0, que permitió la captura, almacenamiento y gestión electrónica de los datos recogidos en el CRD.
El proyecto de esta investigación fue sometido a revisión por el Consejo Científico Institucional y el Comité de Ética de la Investigación Clínica, quienes lo evaluaron desde el punto de vista científico, metodológico y ético. Se determinó que se ajustaba a la Declaración de Helsinki (Principios éticos para las investigaciones médicas en seres humanos, adoptada por la Asamblea Médica Mundial, Seúl 2008). Este estudio y sus procedimientos se llevaron a cabo según lo normado en los códigos nacionales e internacionales de ética y regulaciones legales vigentes en Cuba (Normas de Buenas Prácticas Clínicas, CECMED 2001), así como en la Guía de BPC de la Conferencia Internacional de Armonización. Quedó recogido el modo de protección de derechos y bienestar de los pacientes involucrados y se cumplió con las normas y requisitos mínimos establecidos para la obtención del consentimiento.
Resultados
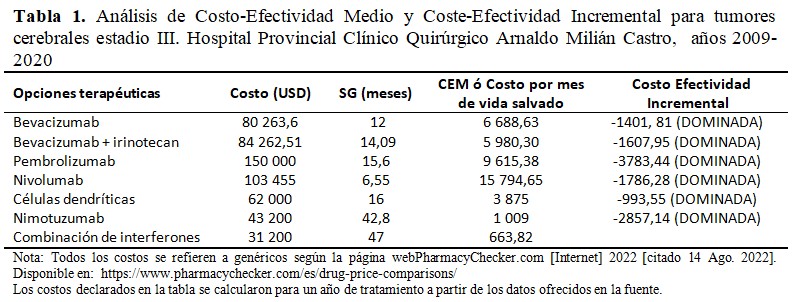
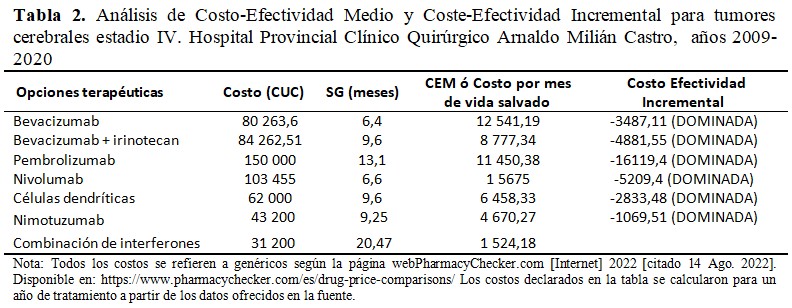
En este caso también se realizó una evaluación económica completa. La tabulación de CEM y CEI se recogieron en la tabla 1 para el estadio III y en la tabla 2 para el estadio IV.
Los esquemas de tratamien-to evaluados son compuestos por medicamentos genéricos, de los cuales solo el nimotuzumab y la combinación de interferones son de fabricación nacional, los costos de los tratamientos se estimaron al multiplicar el costo unitario del medicamento por la unidad de presentación, por la dosis recomendada antes de un ciclo de tratamiento, por un año de tratamiento. (Tabla 1 y Tabla 2).
Discusión
El costo de un año de tratamiento con la combinación de interferones resultó inferior al costo de cualquiera de las opciones terapéuticas internacionales o del nimotuzumab para igual tiempo, evaluados en el estudio, tanto al comparar los casos en estadio III como estadio IV de la enfermedad. La efectividad, evaluada como meses de SG, alcanzada con el producto de investigación fue mayor que todas las descritas para los pacientes en cualquier estadio de la enfermedad. Para los enfermos en estadio III, los resultados con nimotuzumab y con la combinación de interferones son comparables y ambos superiores a los demás genéricos descritos, seguidos por las vacunas de CD y el pembrolizumab. Para los pacientes en estadio IV, solo la combinación de interferones y el pembrolizumab superan los doce meses de SG.
El CEM más bajo y eficiente resultó la combinación de interferones, con 663,82 USD por mes de vida salvado para el estadio III y con 1 524,18 USD por mes de vida salvado para el estadio IV. Los CEM menos eficiente en el estadio III fueron del nivolumab con 15 794,65 USD y el pembrolizumab, con 9 615,38 USD, aunque los resultados de SG descritos para este último pudieran hacer válida esta opción terapéutica. Los CEM menos eficiente en el estadio IV correspondieron al bevacizumab con 12 541,19 USD y de nuevo al pembrolizumab con 11 450,38 USD y valores de SG a considerar para la atención de estos pacientes.
Para relacionar el costo promedio de una intervención en salud, en este caso la combinación de interferones y el beneficio promedio de la misma, comparada con otras variantes, se determina el CEI. Si se considera el bajo nivel de éxito de estas terapias y el largo tiempo que toma su desarrollo, se comprende el manejo de sus costos frente a los estrechos márgenes de eficacia de algunos fármacos o combinaciones en estas entidades, como es el caso del bevacizumab como monoterapia con alrededor de un año de SG, frente a la incorporación del irinotecan, que lleva a un incremento de dos meses de SG y de 4 000 USD por año de tratamiento. Al evaluar el CEI, en todos los análisis para ambos estadios el resultado es negativo, esto ocurre porque la combinación de interferones es menos costosa que cualquiera de las opciones terapéuticas descritas.
Estas estrategias terapéuticas con CEI negativo se consideraron “dominadas”, más costosas y menos efectivas. Debido a que los tratamientos para tumores cerebrales de alto grado de malignidad en recurrencia son mutuamente excluyentes, o sea, la administración de una de estas terapias no se recomienda de forma concomitante con otra, aunque sí pueden ser reemplazadas en la medida que se producen nuevas recurrencias en el paciente, siempre debería elegirse la que ofrece CEI menor.
Se consideró una limitación en el estudio que las dosis de los comparadores y el costo total se contemplaron para un peso corporal normal, se conoce que el peso es un indicador de sensibilidad en los modelos de tratamiento. La presente investigación no pudo determinar por completo el curso natural de la enfermedad en el mundo real para los comparadores, por lo que pudiera no estar reflejada la eficacia de la forma más adecuada para los mismos.
Se han ejecutado varios análisis de costo efectividad y costo utilidad para pacientes con tumores cerebrales de alto grado de malignidad en condiciones de recurrencia. El estudio fármaco-económico y de efectividad del esquema bevacizumab-irinotecan en el tratamiento de las recurrencias del GM primario frente a otras líneas de tratamiento, ejecutado por Ruiz(9) y referido con anterioridad, demostró que aumentar la SG en 4,4 meses para 36 pacientes supuso un importe de 612 506,28 EUR y cada año de SG por paciente, el costo alcanzó la cifra de 46 401,99 EUR. La tesis de Marín(10) sobre la utilización de bevacizumab en pacientes oncológicos, refirió el costo medio de tratamiento en 26 819 EUR, el CEI específico para los gliomas malignos fue de 32 751,75 EUR. Sobre los implantes de carmustina para GMr, Pérez(11) presentó los resultados de una revisión de estudios de costo efectividad en España, que ubicó el costo por paciente entre 44 324 EUR y 44 161 EUR.
El estudio de Connock(12) de comparación de modelos de Markov publicados para la estimación de la rentabilidad en el tiempo de tres estudios de caso de tratamientos para el GM, evidenció diferencias en las estimaciones de CEI, se produjeron apreciaciones poco realistas, ya que los modelos contemplan periodos completos de evaluación de costo, que a menudo no se corresponden con la SG real por individuo.
En la revisión realizada para esta discusión no se encontraron estudios de evaluación fármaco-económica para el pembrolizumab, el nivolumab, la vacunación con CD ni el nimotuzumab. Esto puede deberse al escaso interés de las compañías farmacéuticas en publicar los elevados costos con pobres resultados de sobrevida para estos pacientes.
Se evidenció en el estudio la factibilidad económica del empleo de la combinación de interferones (Heberferón®), al compararlo con otros productos en estudio para tratar a pacientes con tumores cerebrales de alto grado de malignidad sin opciones terapéuticas, al generar el costo más bajo por cada mes de vida salvado.
Conflicto de intereses
Los autores declaran que no existe conflicto de intereses.
Contribuciones de los autores
Conceptualización: María Margarita Ríos Cabrera.
Curación de datos: Javier Cruz Rodríguez.
Análisis formal: María Margarita Ríos Cabrera, Javier Cruz Rodríguez, Iraldo Bello Rivero.
Investigación: María Margarita Ríos Cabrera, Javier Cruz Rodríguez, Iraldo Bello Rivero.
Metodología: María Margarita Ríos Cabrera, Javier Cruz Rodríguez.
Administración del proyecto: María Margarita Ríos Cabrera.
Supervisión: Iraldo Bello Rivero.
Validación: María Margarita Ríos Cabrera.
Redacción-borrador original: María Margarita Ríos Cabrera.
Redacción-revisión y edición: María Margarita Ríos Cabrera, Javier Cruz Rodríguez, Iraldo Bello Rivero.
Financiación
Hospital Provincial Clínico-Quirúrgico Arnaldo Milián Castro. Santa Clara, Cuba.