INTRODUCCIÓN
El dominio de los diversos diseños de investigación (DI) es esencial para abordar eficientemente las incertidumbres en el ámbito clínico. Cada DI posee límites y alcances distintos, y no existe uno único que pueda abordar todas las interrogantes existentes.(1,2) Mientras que un estudio transversal se centra en la prevalencia de una enfermedad en un momento específico,(3) un estudio de cohorte explora la relación entre una exposición y la aparición de una enfermedad a lo largo del tiempo.(4)
La elección adecuada del DI en la investigación clínica es crucial, dada la velocidad de los avances científicos y la variedad de preguntas que emergen constantemente. Es vital diferenciar entre los DI primarios,(2) como los ensayos clínicos aleatorizados(5) y los estudios de cohortes,(4) y la investigación secundaria, representada principalmente por revisiones.(6,7)
Comprender y distinguir entre DI primarios y secundarios es relevante para interpretar y aplicar la evidencia científica adecuadamente.(1,2,7,8) Aunque cada diseño tiene sus ventajas y limitaciones,(1,2,9,10) es fundamental seleccionar aquel que mejor se adapte a la pregunta de investigación y a la incertidumbre clínica en cuestión. Esto, esencialmente, se traduce en entender las diferentes categorías epidemiológicas y cómo se relacionan con los DI.(8)
Al emprender una investigación clínica, la selección del DI no solo se basa en la naturaleza de la pregunta investigativa, sino también en factores prácticos como costos, recursos disponibles y tiempo.
Cada diseño conlleva sesgos y limitaciones inherentes que deben ser considerados con atención.(1) Asegurar la validez, tanto interna como externa, de los estudios es esencial. Por lo tanto, elegir el diseño correcto, llevar a cabo el estudio con meticulosidad y adherirse a directrices internacionales son pasos cruciales para derivar conclusiones robustas. Cada diseño responde a una categoría epidemiológica particular, y tener claridad al respecto es relevante para evitar errores en la elaboración e interpretación de la información científica.(8)
Este manuscrito inicia una serie metodológica que se enfoca en los diseños de investigación más comunes en la Epidemiología Clínica. Buscamos proporcionar a profesionales de la salud y estudiantes una guía clara y práctica, sirviendo como herramienta didáctica y fuente de inspiración para aplicar esta metodología rigurosamente, ya sea en la práctica clínica o en proyectos de tesis.
DESARROLLO
Clasificación de los diseños de investigación: experimentales y observacionales:
Diseños experimentales: los estudios experimentales, comúnmente conocidos como ensayos clínicos aleatorizados (ECA), están específicamente diseñados para abordar cuestiones relacionadas con la terapia/intervención en epidemiología.(1,5,11,12) Su objetivo principal es evaluar la eficacia y seguridad de una intervención en seres humanos.(5,12) Esto se logra al comparar la incidencia de un evento clínico particular (el resultado de interés u “outcome”) en un grupo de individuos con una condición patológica que recibe un tratamiento experimental “x” con respecto a un grupo de control que no recibe dicha intervención.(11,12)
En resumen, los estudios experimentales, como los ECA, desempeñan un papel fundamental en la investigación Biomédica y en la Práctica Basada en la Evidencia (PBE).(12) Estos diseños proporcionan la base para evaluar la eficacia y seguridad de las intervenciones terapéuticas y son esenciales para tomar decisiones clínicas informadas.(5)
La elección cuidadosa del diseño adecuado y la ejecución rigurosa del estudio son cruciales para obtener conclusiones sólidas y para mejorar constantemente la atención médica. Es imperativo que los investigadores, profesionales de la salud y estudiantes, reconozcan la importancia de estos diseños y los utilicen de manera efectiva para avanzar en la PBE y proporcionar la mejor atención posible a los pacientes.
Diseños observacionales: los diseños observacionales se distinguen por su enfoque en la observación de eventos y situaciones sin intervenir o alterar activamente las circunstancias de los sujetos de estudio.(1,2) Estos diseños son valiosos cuando la intervención directa no es ética, factible o práctica.(10) A continuación, se describen algunos de los tipos más comunes de diseños observacionales:(1,2,3,4,13)
- Reporte de casos o serie de casos: estos son descripciones detalladas de la presentación, tratamiento y seguimiento de uno (reporte de caso) o varios (serie de casos) pacientes.(1) Tienen un valor particular en la identificación de novedades o rarezas en la presentación clínica o en la respuesta al tratamiento.(10)
- Estudios transversales: también conocidos como estudios de prevalencia, se llevan a cabo en un punto específico en el tiempo y evalúan la relación entre condiciones de salud y factores de interés en ese momento. Ofrecen una «instantánea» de una situación particular.(2,3)
- Estudios de casos y controles: estos estudios comienzan identificando a individuos con una condición específica (casos) y sin ella (controles).(13) Luego, se investiga de manera retrospectiva para identificar factores o exposiciones que podrían haber contribuido a la aparición de esa condición.(1,2,13)
- Estudios de cohorte: observan a un grupo específico (cohorte) durante un período de tiempo para determinar la incidencia de resultados específicos y cómo estos se relacionan con determinadas exposiciones o factores de riesgo.(1,4)
- Estudios ecológicos: analizan las relaciones en niveles grupales o poblacionales en lugar de individuales.(1,2,10) Por ejemplo, podrían estudiar la relación entre el consumo medio de un alimento y la prevalencia de una enfermedad en diferentes regiones o países.
Es relevante señalar que, aunque los diseños observacionales son valiosos en la investigación epidemiológica, debido a su enfoque no intervencionista, están expuestos a ciertos sesgos que pueden comprometer la validez de los resultados.(2) Uno de los sesgos más preocupantes en estos estudios es el sesgo de confusión, el cual puede surgir debido a la presencia de variables que están asociadas tanto con la exposición bajo investigación como con el resultado estudiado, lo que puede conducir a interpretaciones incorrectas si no se abordan adecuadamente.(9) En esencia, las variables de confusión pueden distorsionar la relación entre la exposición y el resultado, lo que podría llevar a conclusiones erróneas sobre la existencia o la magnitud de una asociación real.(9) Por tanto, es fundamental abordar el sesgo de confusión de manera rigurosa en los estudios observacionales. Esto implica implementar estrategias en la fase de diseño y análisis del estudio para controlar o ajustar posibles factores de confusión.(9) Los investigadores deben estar conscientes de este riesgo y tomar medidas proactivas para minimizar su impacto, ya que esto contribuye a obtener resultados más confiables y una interpretación más precisa de las asociaciones entre la exposición y el resultado estudiado.
Categorías epidemiológicas y su influencia en la elección de diseños de investigación:
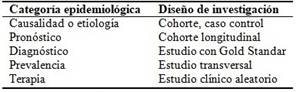
El cuadro 1 muestra una relación clara entre las diferentes categorías epidemiológicas y su influencia en la selección de los DI adecuados.(8) En resumen, si queremos entender la causalidad o etiología de una enfermedad, debemos enfocarnos en estudios de cohorte o casos y controles, que son especialmente efectivos para establecer relaciones causa-efecto. Por otro lado, si nuestro objetivo es analizar el pronóstico de una enfermedad, el diseño de cohorte longitudinal es la mejor opción.(1,4,8) Además, las categorías epidemiológicas de diagnóstico, prevalencia y terapia también son importantes al momento de elegir los diseños adecuados para abordar preguntas específicas en el ámbito de la epidemiología.(8) Esta conexión entre las categorías epidemiológicas y los DI brinda una guía esencial para los investigadores, clínicos y estudiantes al seleccionar la metodología más adecuada para abordar sus preguntas de investigación y obtener resultados sólidos. (Cuadro 1).
Recursos y disponibilidad de tiempo
Cuando se elige un DI, es importante tener en cuenta varios factores para asegurarse de que sea apropiado para abordar una pregunta de investigación específica.(8) Estos factores pueden afectar la duración del estudio, el costo y la infraestructura necesaria para llevar a cabo la investigación. La duración del estudio es un aspecto crítico que varía según el diseño de investigación seleccionado.(2) Por ejemplo, los estudios longitudinales o de cohorte pueden requerir seguimientos a largo plazo para capturar cambios y tendencias significativas a lo largo del tiempo.(1,2,4) Por otro lado, los estudios transversales(1,3) se realizan en un momento específico y son más adecuados cuando se busca una instantánea de la situación en ese momento. El costo es otro factor importante a considerar. En general, los estudios experimentales tienden a ser más costosos debido a la necesidad de controlar y manipular variables, lo que puede requerir recursos adicionales.(1,2,3,5,12) Además de los costos directos, también se deben tener en cuenta otros recursos, como la disponibilidad de personal capacitado, equipos especializados y acceso a poblaciones o datos específicos.
La infraestructura disponible también puede influir en la elección del diseño de investigación. Por ejemplo, llevar a cabo un estudio en un entorno clínico controlado puede requerir una infraestructura más compleja en comparación con un estudio de encuesta que se puede realizar con recursos más limitados. Por lo tanto, es esencial evaluar la infraestructura disponible y su capacidad para respaldar el DI seleccionado. En resumen, al seleccionar un DI, es crucial considerar la duración del estudio, el costo y la infraestructura necesaria. Estos factores garantizarán que el diseño elegido sea adecuado para abordar la pregunta de investigación de manera efectiva y eficiente.
Consideraciones éticas
Las consideraciones éticas desempeñan un papel crucial en la investigación clínica al asegurar la integridad y el respeto hacia los participantes.(14,15) Al diseñar y llevar a cabo estudios en seres humanos, es necesario considerar diversos aspectos clave. La ética adquiere una relevancia especial cuando se trata de intervenciones en seres humanos, ya que no todas las intervenciones son éticamente aceptables para ser probadas en humanos, especialmente si existen pruebas previas de posibles daños o si se priva a los participantes de un tratamiento estándar reconocido.(14)
Por lo tanto, es vital realizar un análisis ético detallado de cada intervención propuesta, priorizando la protección de los derechos y el bienestar de los participantes.(14,15) Además, se debe prestar especial atención a las poblaciones vulnerables, como niños, embarazadas o personas con discapacidades cognitivas, ya que estas poblaciones requieren consideraciones éticas adicionales debido a su vulnerabilidad y la necesidad de garantizar su protección.(14) Los protocolos de investigación deben abordar adecuadamente las necesidades y derechos de estas poblaciones, asegurando la obtención de un consentimiento y/o asentimiento informado apropiado y ético.(15)
En el caso de estudios que recopilan datos retrospectivos, se presentan dilemas éticos, especialmente si no se obtuvo consentimiento en el momento original o si existe un riesgo para la privacidad de los participantes.(16) En tales situaciones, es esencial seguir procedimientos éticos adecuados para obtener el consentimiento informado o demostrar que la recopilación de datos retrospectivos es ética y legalmente aceptable.(14,15,16,17).
La evaluación de los posibles beneficios en comparación con los riesgos para los participantes es un elemento fundamental en cualquier investigación.(17) Esta evaluación es esencial para determinar la viabilidad ética de un estudio y garantizar que los participantes estén debidamente informados y protegidos.
Los comités de ética en la investigación juegan un papel crucial en el ámbito de la investigación clínica al encargarse de revisar y aprobar los protocolos de estudio.(14,15,16,17,18) Su principal función es asegurar el cumplimiento de los más estrictos estándares éticos en la investigación médica. La revisión realizada por estos comités es un paso crítico para asegurar la ética y el apego a los principios de respeto, beneficencia y justicia.(14,15,16,17)
El trabajo de estos comités no solo es una exigencia regulatoria, sino también un compromiso moral y ético con los participantes de la investigación y la sociedad en general.(14,16) A través de una evaluación minuciosa, buscan garantizar el respeto a los derechos y la dignidad de los participantes.(14,15,16,17,18) Esto implica asegurarse de que los participantes brinden un consentimiento informado y voluntario, estén protegidos de riesgos innecesarios y reciban los beneficios de la investigación de manera equitativa.(14) Además de salvaguardar los derechos de los participantes, los comités de ética también evalúan la calidad científica y la validez del diseño del estudio. Esto es fundamental para garantizar que la investigación cumpla con altos estándares científicos y contribuya significativamente al conocimiento médico.
La revisión de los comités de ética no se limita solo a la aprobación inicial de los protocolos, sino que también desempeñan un papel continuo en la supervisión y seguimiento de la investigación.(14,16) Están atentos a cualquier cambio en el protocolo o circunstancias que puedan afectar la ética de la investigación y toman las medidas necesarias para abordar cualquier problema ético que surja durante el estudio.(14,16,17) En resumen, los comités de ética en la investigación son guardianes de la integridad y la ética en la investigación clínica. Su labor es esencial para garantizar la investigación ética, respetando los derechos de los participantes y cumpliendo con los principios de respeto, beneficencia y justicia. Su contribución es vital para el avance de la ciencia médica y la protección de la sociedad en general.(14,15,16,17,18)
CONCLUSIONES
Los DI son esenciales en la investigación clínica, determinando la solidez y aplicabilidad de los hallazgos. Estos no solo son fundamentales para la PBE, sino también para impulsar descubrimientos que beneficien a los pacientes. A través de la clasificación en diseños experimentales y observacionales, y enfatizando las consideraciones éticas, los DI contribuyen a una investigación clínica más robusta y ética. La elección adecuada y la aplicación rigurosa de los DI son determinantes para avanzar en medicina y beneficiar a la sociedad.
Conflicto de intereses
Los autores declaran la no existencia de conflicto de intereses.
Contribuciones de los autores
Conceptualización de ideas: Raúl Aguilera-Eguía; Ángel Roco-Videla; Olga Patricia López Soto.
Investigación: Raúl Aguilera-Eguía; Ángel Roco-Videla; Olga Patricia López-Soto; Brenda Herrera Serna.
Redacción: Raúl Aguilera-Eguía; Ángel Roco-Videla; Olga Patricia López-Soto; Brenda Herrera Serna; Georgiy Polevoi Polevoi; Héctor Fuentes Barria; Mariana Melo-Lonconao.
Redacción, revisión y edición: Raúl Aguilera-Eguía; Ángel Roco-Videla; Olga Patricia López-Soto; Brenda Herrera Serna; Georgiy Polevoi Polevoi; Héctor Fuentes Barria.
Financiación
Sin financiamiento externo.