INTRODUCCIÓN
El ictus constituye un grave problema de salud pública a nivel mundial. La Organización Mundial de la Salud lo ubica como la segunda causa de mortalidad en importancia a nivel global, responsable del 11,9 % del total de muertes.(1) Las sepsis son una complicación frecuente en la fase aguda del ictus; los índices de reportes varían considerablemente entre 5-65 %.(2) La neumonía es la infección post-ictus más frecuente, con un profundo efecto en el desenlace clínico al triplicar el riesgo de morir en este grupo de pacientes. Suele ocurrir con más frecuencia dentro de los primeros siete días tras el debut del evento,(3) ya que refleja de manera considerable el período de mayor riesgo en términos de prevalencia de disfagia, inmovilidad, deterioro del nivel de conciencia y supresión de la respuesta inmune.(3,4)
La infección afecta el pronóstico del ictus por varias razones: prolongación de la inmovilización, mayor fragilidad y retraso en la rehabilitación por mayor estancia hospitalaria, e incremento considerable del coste del proceso.(5) Según datos de un estudio estadounidense, el ictus, para pacientes con neumonía, tendría un coste adicional de más de 14 836 dólares; además, los pacientes con neumonía necesitarían una extensión de los cuidados.(5) Según los meta-análisis, la incidencia global de neumonía en pacientes con ictus agudo se encuentra alrededor del 14,3 %, con una heterogeneidad importante entre los estudios realizados debido al tipo de población en investigación, al tipo de diseño y a las variaciones en la definición de neumonía postictus.(2,3) Recientemente, varias investigaciones han identificado factores de riesgos independientes para el desarrollo de la neumonía asociada al ictus,(5,6) varios de los cuales han sido incluidos en sistemas de escalas de puntuación para predecir su ocurrencia.(7)
Además del proceso inflamatorio local del cerebro, el ictus también altera el sistema inmunológico, con lo que provoca una predisposición de los pacientes a la inmunodepresión, y a las infecciones (principalmente neumonías e infecciones del tracto urinario), lo que se ha denominado inmunodepresión postictus.(8) Ese estado de inmunodepresión, unido a la estimación del estado nutricional al ingreso mediante parámetros analíticos relacionados con el estado nutricional (albúmina, colesterol total y linfocitos totales),(9) y los demás factores de riesgo identificados, pudieran estar también relacionados con el desarrollo de esta complicación. Hasta donde hemos investigado, no se dispone en Cuba de un instrumento para predecir la aparición de la neumonía asociada al ictus isquémico agudo (NAIIA), motivo por el cual se realiza la presente investigación, con el objetivo de elaborar un índice para tales fines, ajustado a las características de nuestra población.
MÉTODOS
Se realizó un estudio comparativo, basado en una cohorte prospectiva de pacientes con diagnóstico clínico y por tomografía axial computarizada de infarto cerebral isquémico agudo, atendidos en el Hospital General Universitario Carlos Manuel de Céspedes, del municipio Bayamo, provincia de Granma, desde el 1ro. de enero de 2016 hasta el 31 de diciembre de 2018. Para el diagnóstico del ictus isquémico agudo (IIA) se tuvo en cuenta los criterios diagnósticos de la actual Guía Cubana de Práctica Clínica para la Enfermedad Cerebrovascular.(10)
Fueron incluidos todos los adultos de 18 años o más, que ingresaron en el centro hospitalario de IIA; y excluidos los pacientes con tuberculosis pulmonar, sida definido, las gestantes, así como los pacientes con recolección insuficiente de datos. Todos tuvieron al IIA como principal diagnóstico de hospitalización; como criterios de salida, pacientes en los cuales no fue posible obtener la totalidad de los datos para la investigación, por fallecimiento o dificultades en su seguimiento.
La muestra de construcción del índice estuvo integrada por 375 pacientes mayores de 18 años de edad, de los cuales 179 (47,7 %) tenían más de 70 años de edad, 217 (57,9%) pertenecían al sexo masculino y 83 (22,1 %) desarrollaron la NAIIA. Se consideró NAIIA según los criterios actuales vigentes para su diagnóstico.(11)
Criterios clínicos (Presencia de al menos uno de los siguientes criterios pasadas las primeras 48 horas).
1. Fiebre > 38 grados centígrados sin otra causa reconocida.
2. Leucocitosis ≥ 12 000/mm3 o leucopenia < 4 000/mm3.
3. Adultos ≥70 años con alteración del estado mental sin otra causa reconocida.
Más al menos dos de los siguientes criterios.
1. Aparición de un nuevo esputo purulento, o cambio en las características del esputo (color, olor, cantidad y consistencia) en un período de 24 horas, o incremento de las secreciones respiratorias, o incremento en la necesidad de aspiraciones.
2. Nuevo episodio de tos, disnea o taquipnea (FR >25/min).
3. Auscultación sugestiva: crepitantes, roncos, sibilancias.
4. Deterioro del intercambio gaseoso (desaturación de O2 [ejemplo, PaO2/FiO2≤ 240] o aumento de las demandas de O2 o de la demanda ventilatoria).
Y ≥2 radiografías seriadas de tórax con al menos uno de los elementos siguientes criterios: infiltrado persistente nuevo o progresivo, consolidación o cavitación.
En pacientes sin enfermedad cardiaca o pulmonar una radiografía de tórax fue suficiente.
Criterio microbiológico:
A) Uso de algún método microbiológico alternativo: 1) Hemocultivo positivo no relacionado con otro foco de infección, 2) Crecimiento positivo en cultivo de líquido pleural, 3) Evidencia de neumonía en examen histológico pulmonar.
B) Cultivo positivo de esputo o no cuantitativo de muestra de tracto respiratorio inferior.
Variable analizadas: NAIIA; edad (años cumplidos); escala de NIHSS (puntos), cifras de hemoglobina, plaquetas, colesterol, albúmina, conteo global linfocitos, proteínas totales, urea, creatinina; sexo (masculino/femenino), hábito de fumar (si/no), historia de enfermedad pulmonar obstructiva crónica (EPOC) (si/no), alcoholismo (si/no), fibrilación atrial (si/no), insuficiencia cardiaca (si/no), ictus previo (si/no), presencia de afasia motora/disartria (si/no), disfagia (si/no), uso de antibiótico en los últimos 30 días (si/no).
Para la identificación de los factores de riesgo con influencia independiente de la aparición de la NAIIA, se realizó un estudio multivariado mediante la técnica de regresión logística binaria.
Construcción y validación del modelo de predicción: Una vez identificados los factores de riesgo con influencia independiente se procedió a la creación del índice predictivo. Se consideró que este debía estar formado por ítems que se integrarían en un índice global que tomaría la forma de una combinación lineal entre los ítems. A cada una de las variables retenidas por el modelo generado mediante la regresión logística, se le asignó el puntaje de su coeficiente de regresión (se aproximó a números enteros). Una vez confeccionado el índice predictivo se sometió a un estudio de eficacia diagnóstica y se generaron curvas receptor- operador (ROC, por sus siglas en inglés).
Validez de construcción: La asociación entre el índice ordinal y la morbilidad se evaluó a partir de la prueba de Ji cuadrado y el coeficiente de asociación Eta (η); los valores promedio entre los pacientes con NAIIA y sin esta, mediante la prueba no paramétrica U de Mann-Whitney para muestras independientes.
Este proceso se realizó con el algoritmo incluido en el paquete estadístico SPSS en su versión 18.0 para Windows.
Antes de ser incluidos en el estudio se solicitó a cada paciente, o en su defecto (en caso de deterioro importante de nivel deconciencia o afasia severa), al familiar, su consentimiento informado verbal y escrito. El estudio fue aprobado por el Consejo Científico y Comité de Ética del Hospital.
RESULTADOS
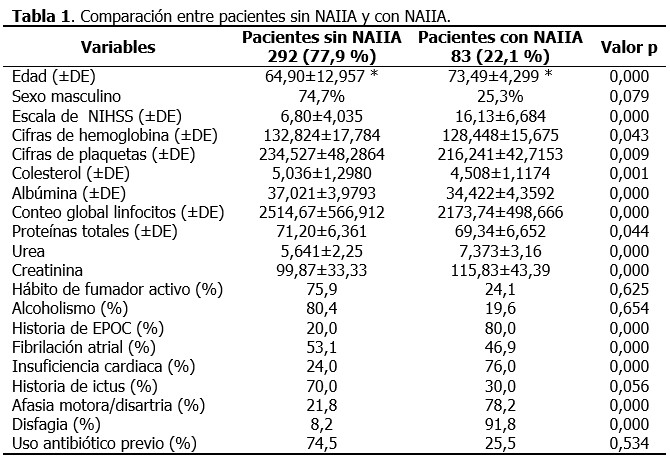
Al comparar ambos grupos de pacientes con respecto a las variables en estudio, las diferencias más significativas se observaron en la edad, la puntuación en la escala de NIHSS, y las cifras iniciales de albúmina, urea, creatinina y conteo global linfocitos. Con relación a la comorbilidad preexistente se identificó diferencia significativa con relación a la historia previa de EPOC, insuficiencia cardiaca, fibrilación atrial, así como la presencia al ingreso de disfagia y afasia motora/disartria severa. (Tabla 1).
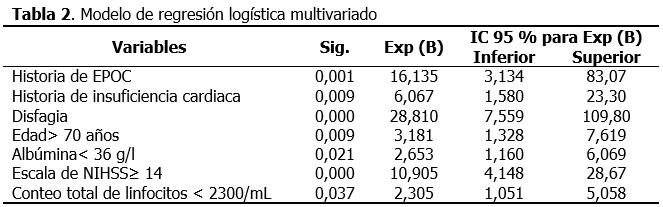
Fueron identificadas siete variables con influencia independiente sobre al pronóstico de NAIIA, entre ellas sobresalieron la disfagia (Exp (B) 28,8; IC 95 % 7,5-109,8), el antecedente de EPOC (Exp (B) 16,1; IC 95 % 3,1-83,0), y una puntuación de NIHSS≥ 14 (Exp (B) 10,9; IC 95 % 4,1-28,6). Otros factores identificados fueron la historia de insuficiencia cardiaca, la edad> 70 años, la albúmina< 36 g/l y el conteo total de linfocitos < 2300/mL. (Tabla 2).
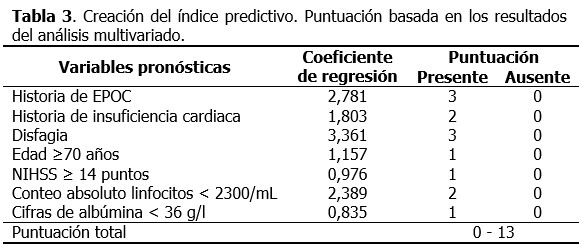
El índice construido a partir del modelo de regresión logística multivariado contó con 7 variables. Las mayores puntuaciones estuvieron relacionadas con la presencia de disfagia y la historia de EPOC. (Tabla 3).
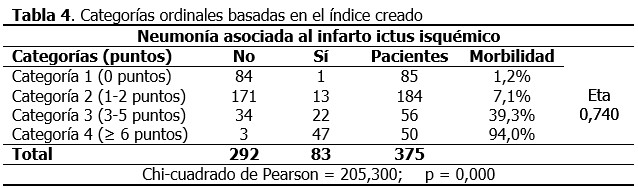
Al analizar la creación de categorías ordinales de riesgo, basadas en el índice construido y su relación con riesgo de NAIIA, se encontró una excelente asociación (coeficiente Eta 0,740), donde 94,0 % de los pacientes con alto riesgo de desarrollar NAIIA fueron clasificados en la categoría 4. (Tabla 4).
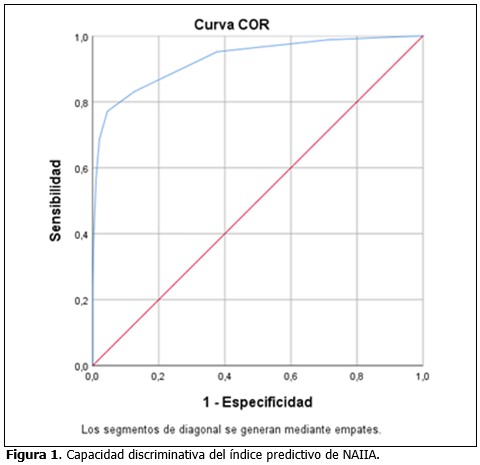
Cuando se probó la capacidad de predecir la NAIIA, estimada con la función obtenida por el modelo de regresión, se encontró un área bajo la curva ROC significativamente mayor de 0,75 (0,928; IC: 95 %; 0,894-0,963). (Figura 1, Tabla 5).
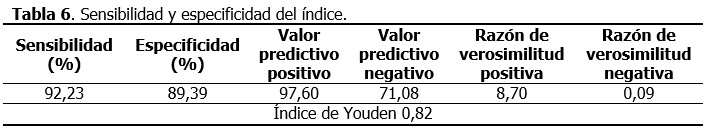
La capacidad del índice para detectar un sujeto enfermo fue de 92,23 %; la probabilidad condicional de que los individuos con la prueba positiva tuvieran realmente la enfermedad fue del 97,60 %. Los enfermos tuvieron 8,70 veces más probabilidad de que el índice los diagnosticara con NAIIA. La veracidad de la prueba fue documentada por un índice de Youden cercano a uno (0,82). (Tabla 6).
DISCUSIÓN
Los ensayos clínicos realizados hasta el momento para evaluar si la antibioticoterapia preventiva mejora las tasas de infección no han tenido la suficiente potencia para lograr su cometido.(13) Identificar a los pacientes que en el momento del ingreso tienen un mayor riesgo de sufrir una infección respiratoria aguda (IRA) tras el ictus, puede ayudar en el manejo de este proceso y tratar las infecciones de forma precoz.(2,12) Con el objetivo de mejorar la identificación de los pacientes con un alto riesgo de sufrir NAIIA se han diseñado varios modelos de predicción; estos deben estar basados en marcadores patogénicamente relevantes, que estén presentes en las primeras 24 horas, y sean sencillos de conseguir.(13-18) En los últimos años se han publicado diferentes modelos predictivos, como, por ejemplo: A2DS2 score,(14) ISAN score,(15) ACDD4 score,(16) AIS-APS score,(17) y PANTHERIS score.(18) En todas estas escalas coinciden marcadores patogénicos como la gravedad del ictus medido mediante la escala NIHSS, la disfagia, la edad, la historia de EPOC e insuficiencia cardiaca, entre otros; sin embargo, los autores de la presente investigación consideran que debería evaluarse la influencia de otros marcadores patogénicos que, a la luz de las más recientes investigaciones, han demostrado su relación con el desarrollo de la NAIIA, tal es el caso de la inmunodepresión mediada por ictus(9,19) y la evaluación del estado nutricional inicial,(20) éste último medido mediante las cifras de albúmina, colesterol total y el conteo global de linfocitos, las cuales son de fácil obtención en las primeras 24-48 h. Teniendo en cuenta lo anterior, se optó por evaluar el comportamiento e interacción de estas últimas variables con el resto de las variables identificadas en las escalas anteriormente descritas.
La escala diseñada incluye siete variables: historia de EPOC, historia de insuficiencia cardiaca, la disfagia, edad ≥70 años, NIHSS ≥ 14 puntos, conteo absoluto linfocitos < 2300/mcL, y cifras de albúmina < 36 g/l. De estas, la disfagia es el único parámetro que puede tener cierta variabilidad en su forma de medirse, y cuyo diagnóstico puede tener mayor complejidad; la frecuencia de disfagia depende del método de diagnóstico, y resulta superior si se utiliza una evaluación instrumental (videofluoroscopia o nasofibrolaringoscopia), que si se utilizan técnicas de cribado o de evaluación clínica.(21) El conteo absoluto de linfocitos < 2300/mcL, y cifras de albúmina < 36 g/l son dos factores que se incorporan a esta nueva propuesta de índice para predecir la NAIIA, y que está claramente explicada por los eventos que fisiopatológicamente acontecen, tanto a nivel inmunológico local en el cerebro, como a nivel sistémico en este grupo de enfermos, además del cribado nutricional habitual que se debe practicar a cada paciente hospitalizado.
Para el diseño del índice se tuvieron en cuenta los aspectos metodológicos documentados para este tipo de herramienta,(22) y para la validez de presentación y contenido se efectuó una exhaustiva revisión bibliográfica.
El índice propuesto posee una excelente capacidad para predecir la aparición de NAIIA, lo cual está avalado por las cifras de sensibilidad y especificidad alcanzadas, y reafirmado por los excelentes valores predictivos, así como también por la razón de verosimilitud positiva y la calibración. Por su parte, la asociación entre el riesgo de NAIIA y la escala propuesta es muy buena, dada la correspondencia entre las puntuaciones más altas de esta con la probabilidad de desarrollar NAIIA, lo cual es evidente al observar los valores del coeficiente Eta. Las variables en las que se basa el índice son factores de importancia en el desarrollo de la NAIIA, y los valores asignados a cada uno de ellos están en consonancia con el peso fisiopatológico de estos en la génesis de la entidad.(2,4,19,20) La validez de construcción del índice quedó demostrada al evidenciarse que la mayoría de los pacientes que desarrollaron la NAIIA se encuentran en las categorías de mayor riesgo, lo cual se fundamenta, además, por el hecho de que los factores empleados en la construcción del índice están vinculados con la patogenia de la NAIIA. Corresponde someter este nuevo índice a un proceso de validación tanto interna como externa.
Se concluye que el índice formulado está compuesto por parámetros fiables, fácilmente disponibles y rápidos de aplicar en las primeras 24-48 horas del IIA, y permite predecir el desarrollo de la NAIIA.
Conflicto de interés: los autores declaran que no existen plagios, conflictos de interés ni conflictos éticos.
Contribución de los autores: idea conceptual: Alexis Suárez Quesada; recogida del dato primario: Alexis Suárez Quesada, Alexis Álvarez Aliaga, Andrés Quesada Vázquez; análisis estadístico: Alexis Suárez Quesada, Andrés Quesada Vázquez, Alexis Álvarez Aliaga; revisión de la literatura: Alexis Suárez Quesada, Alexis Álvarez Aliaga; escritura del artículo: Alexis Suárez Quesada, Andrés Quesada Vázquez; revisión crítica: Alexis Álvarez Aliaga.
Financiación: la investigación no contó con financiamiento externo.