INTRODUCCIÓN
Dentro de las numerosas aplicaciones médicas de la citogenética, el diagnóstico prenatal citogenético (DPC) constituye tal vez el punto más crítico, debido a que de sus resultados se deriva una importante decisión para la familia: continuar o no un embarazo.1,2
La mayor parte de las alteraciones cromosómicas sucede en parejas con cromosomas sanos y se originan como eventos nuevos, casi siempre durante la gametogénesis. Se estima que del 18 al 19 % de los ovocitos y del 3 al 4 % de los espermatozoides son aneuploides, por lo que no es sorprendente que una de cada 13 concepciones tenga alteraciones cromosómicas con implicaciones médicas, económicas y sociales.3,4
El síndrome de Patau o síndrome de Bartholin-Patau, también conocido como trisomía 13, es una enfermedad genética que resulta de la presencia de un cromosoma 13 suplementario (consecuencia de una no disyunción meiótica, principalmente en el gameto materno). Aproximadamente un 20 % de casos se deben a translocaciones, dentro de las cuales, la t(13q;14q) es la más frecuente. Solo un 5 % de dichas translocaciones es heredada de uno de los progenitores. Los mosaicos representan 5 % de los casos de trisomía 13.5 Es la trisomía reportada menos frecuentemente en la especie humana.5-8 Fue observada por primera vez por Thomas Bartholin en 1657, pero no fue hasta 1960 cuando la describió Patau.9 El tiempo promedio de supervivencia de los niños afectados es de siete días. El 90 % muere durante el primer año de vida,8-10 en dependencia del tipo de anomalías asociadas, pues las malformaciones cardíacas y del sistema nervioso central son las causas de la elevada mortalidad.8,10 Se cree que entre el 80-90 % de los fetos no llegan a término y presentan anomalías múltiples que pueden ser detectadas prenatalmente por medio de la ecografía, el diagnóstico se confirma a través de estudio cromosómico.5-7, 9
La prevalencia de la trisomía 13 es de aproximadamente 1:12 000 nacidos vivos.5,8,11 Cuanto mayor sea la pareja, más probabilidad tienen de engendrar un hijo que presente dicho síndrome. El riesgo de recurrencia (de tener un segundo hijo con síndrome de Patau) es bastante bajo en el caso de que ningún padre presente una translocación.5,11
Constituye la cuarta alteración más frecuente diagnosticada prenatalmente, antecedida por la trisomía 21, la trisomía 18 y la monosomía 45,X0.8 Presenta características fenotípicas muy amplias que incluyen holoprosencefalia y alteraciones craneofaciales como microcefalia (más del 50 %), hendidura labial y/o hendiduras palatinas (entre el 60 y 80 %),8,10 puede encontrarse también ciclopía, arrinia y presencia de proboscis.8 y 10 Se reporta además polidactilia (76 %), pliegue palmar único (64 %), macroftalmias, colobomas, displasia de la retina, sordera, entre otros. En el sistema cardiovascular pueden presentar persistencia del conducto arterioso (80 %), defectos del septo ventricular (80 %), defectos del septo atrial (80 %), implantación baja de las orejas.7,8, 10,12
Otras anomalías frecuentes son los defectos del cuero cabelludo y los senos dérmicos. En la parte posterior del cuello suelen existir pliegues cutáneos laxos. Los genitales suelen ser anormales en ambos sexos: en los niños suele haber criptorquidia y un escroto anormal y las niñas tienen un útero bicorne. En las primeras semanas de vida suele haber crisis de apnea. El retraso mental es grave.3-5,13,14 La mayoría de los pacientes (70 %) muestran una afectación tan grande que mueren antes de los seis meses, de forma que el porcentaje que sobreviven más de 1 año no alcanza el 10 %.6, 7,11
Por lo infrecuente del caso y lo importante del diagnóstico citogenético para corroborar los hallazgos ultrasonográficos, se decidió la presentación de este caso.
PRESENTACIÓN DEL CASO
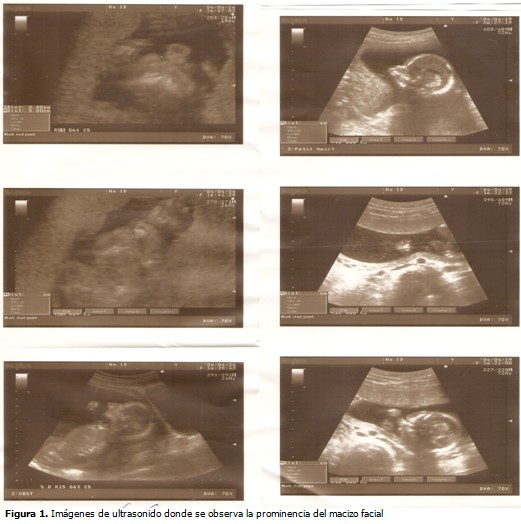
Gestante de 19 años, de procedencia rural, G1, P0, A0, con antecedentes de salud aparente, que fue remitida al Centro Provincial de Genética Médica de Cienfuegos a las 12,3 semanas de la gestación por sospecha de translucencia nucal aumentada, en ultrasonido de primer trimestre realizado en su área de salud. Al realizarse el estudio no se detectó translucencia, pero se observó una prominencia en el macizo facial (probóscide). Se realizó seguimiento evolutivo durante tres semanas, con sospecha de una posible trisomía del cromosoma 13, también conocida como síndrome de Patau. Se repitió el ultrasonido y fue visto por varios especialistas que coincidieron con el diagnóstico. (Figura 1).
Por los indicios observados se le propuso a la paciente la realización de un diagnóstico prenatal citogenético (DPC), lo cual aceptó. En el ultrasonido previo a la toma de muestra de la amniocentesis se observó asimetría de las cuatro cavidades cardíacas, la cual fue corroborada por una ecocardiografía realizada por un cardiólogo.
El DPC, realizado a las 18 semanas de gestación, dio como resultado un cariotipo 47,XX, +13, en coincidencia con la sospecha del diagnóstico por ultrasonido. Se le informó a la paciente el resultado y se le brindó asesoramiento genético, después del cual ella optó por la interrupción del embarazo.
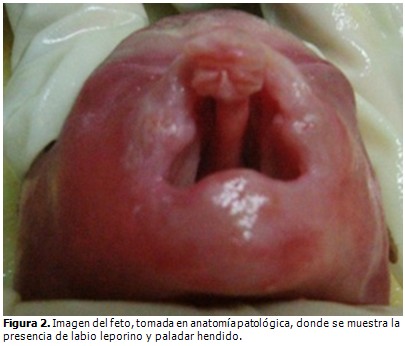
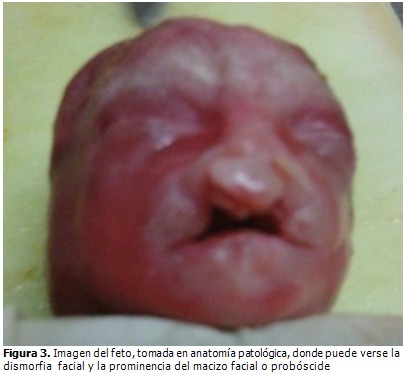
El informe de anatomía patológica concluyó que se trataba de un aborto por eugenesia de un feto femenino que medía 22 cm de talla y brazada, color de la piel rosada intensa, a nivel del labio superior se observó orificio que se continuaba hacia la porción superior de la boca por ausencia del paladar duro (labio leporino acompañado de paladar hendido). Presentaba además polidactilia en la mano izquierda (seis dedos); cardiopatía congénita dado por aorta disminuida de calibre y dextropuesta, hipoplasia cavidades izquierdas, comunicación intraventricular media con ductus amplio y permeable. Pudo apreciarse también la prominencia en el macizo facial o probóscide. (Figuras 2 y 3).
La paciente fue informada del interés en publicar este caso y aceptó firmar un consentimiento informado.
DISCUSIÓN
El síndrome de Patau o trisomía 13, a pesar de su baja frecuencia, presenta una gran cantidad de malformaciones,8 varias de las cuales pueden ser diagnosticadas por ultrasonido. El estudio cromosómico, junto con el informe anátomo patológico pueden servir para confirmar el diagnóstico, como ocurrió en este caso. Según la bibliografía consultada el diagnóstico a través de ecografía en 2 dimensiones puede confirmarse por ecografía de detalle anatómico y estudio tridimensional multiplanar, con lo cual se gana en precisión de detalles no solamente craneales y faciales sino en el resto de la anatomía fetal.8
En el Centro Provincial de Genética Médica de Cienfuegos se realiza el diagnóstico ecográfico con dos dimensiones con el cual se logró realizar un diagnóstico certero. El estudio citogenético fue realizado en el laboratorio, aunque no se pudo obtener una foto del cariotipo. El riesgo de recurrencia de la trisomía 13 libre es muy bajo, se ha estimado entre 0, 5 % y 1 %; en una serie japonesa de 46 mujeres que habían tenido un hijo con trisomía 13, en ninguna hubo recurrencia.8
Dentro de las posibles causas de la trisomía se asocia la edad materna avanzada, que puede ocasionar una no disyunción materna durante la meiosis I en un 90 % de los casos. El riesgo para embarazos a término a los 40 años se estima entre 1:2000 a 1:2638; mientras que para embarazos a término en mujeres de 20 años es de 1:42 423. Un 10 % de los casos se deben a alteraciones de origen paterno.13
Es la tercera trisomía más frecuente entre los nacidos vvos y muestra uma leve predilección por el sexo femenino sobre el masculino 1:0,8, respectivamente.9, 12
Los defectos cromosómicos son una causa importante de enfermedad y mortalidad en el feto, ya que producen abortos espontáneos, óbitos, muerte neonatal, malformaciones congénitas, así como retraso mental; por lo que es de vital importancia el diagnóstico precoz de cualquier defecto cromosómico en el feto ya que así se podrá valorar la posibilidad de tratamiento intrauterino, interrupción del embarazo o preparación del núcleo familiar y del personal de salud, para la atención óptima del neonato afectado, con el fin de minimizar el daño y mejorar el tratamiento o la rehabilitación.3, 12-16
A pesar de no contar con un equipo de ultrasonido en tres dimensiones y el equipamiento para conservar la imagen del cariotipo, nuestros hallazgos citogenéticos y ultrasonograficos fueron corroborados con el informe de anatomía patológica. En nuestro caso se observó, a nivel del labio superior un orificio que se continuaba hacia la porción superior de la boca por ausencia del paladar duro (labio leporino acompañado de paladar hendido), polidactilia mano izquierda (seis dedos); cardiopatía congénita dado por aorta disminuida de calibre y dextropuesta, hipoplasia cavidades izquierdas, CIV basal media con ductus amplio y permeable. Pudo apreciarse también la prominencia en el macizo facial o probóscide, estos hallazgos craneofaciales entre otros, se corroboran con estudios realizados en Chile, Granada, Colombia, Perú.8,10,17,18
Llama la atención que aunque estos casos tienen una esperanza de vida casi nula, en la Isla de la Juventud existe un reporte de una niña de 13 años que aun vive con la enfermedad5 y en Ciego de Ávila se reporta otra niña que al momento del estudio tenía 18 meses.9 En la literatura se reportan pocos casos con supervivencia de más de un año, por ejemplo: Betancourt Castellanos y colaboradores citan que Marden y Yunes publicaron en 1967 el caso de una niña que vivió 10 años.9 También se reporta en el Smith un caso de un paciente adulto de 33 años.19
Fajardo Tornés y colaboradores citan que Lehman describió una frecuencia de aparición de diferentes alteraciones en la trisomía 13: holoprosencefalia 39 %, anormalidad del SNC 58 %, anomalias faciales 48 %, defectos cardiacos 48 %, defectos renales 33 %, polidactilias 40 %, malrotación intestinal 8 %.20
Estos cambios morfológicos descritos de manera aislada pueden sugerir el diagnóstico de alteración cromosómica, aun en restos de legrado endometrial postaborto, y alertar a los médicos para el adecuado abordaje del futuro obstétrico de la paciente, en especial en quienes no sea posible la realización de estudios citogenéticos. Los hallazgos descritos son útiles para dar una aproximación diagnóstica y, de esta manera brindar una asesoría genética a los padres y familiares.