INTRODUCCIÓN
La hemoglobina (Hb), componente fundamental de las células rojas sanguíneas, es el soporte en la transferencia de O2 de los pulmones a los tejidos periféricos, además es la encargada del transporte de CO2 de estos tejidos hasta los pulmones para su posterior excreción, y de colaborar con el mantenimiento del pH sanguíneo. La composición de Hb de un adulto sano tiene diferentes fracciones: componente mayor (Hb A (α2β2) ≥ 96,5 %), componente menor (Hb A2 (α2δ2) ≤ 3,5 %) y componente de origen fetal (HbF < 2 %). Las hemoglobinopatías, enfermedades genéticas con un modo de herencia autosómico recesivo, son alteraciones cualitativas o cuantitativas de la molécula de Hb. El laboratorio de electroforesis de hemoglobina del Centro Nacional de Genética Médica (CNGM), es el responsable de realizar las determinaciones de variantes de hemoglobina de las muestras de sangre en gestantes y sus respectivos esposos en la provincia de Artemisa; además se encarga del control de calidad del programa a nivel nacional. Para mejorar los resultados de este programa se introdujo la tecnología Hydrasys, pero la estabilidad de las muestras es muy importante para lograr la confiabilidad de los resultados.1-4
El procedimiento de los puntos de extracción y recogida de muestras en toda la Red de Genética Médica, ha provocado que las fluidos biológicos se transporten y conserven en condiciones que pueden afectar la estabilidad de varias de las propiedades físico-químicas de sus componentes, provocando que el resultado obtenido sea significativamente diferente del resultado que se obtendría si la muestra se preparase y procesase en condiciones idóneas. El fluido biológico de elección para la realización de esta técnica es sangre total con un anticoagulante añadido, ya sea heparina o EDTAK2, siendo este último el de elección para lograr un análisis y resultados con gran calidad.5
En el primer semestre del año 2012, de un total de 2492 muestras estudiadas, 220 fueron rechazadas, por no presentar las condiciones físico-químicas requeridas. Este problema se fue agudizando a medida que se recibían las muestras y trajo consigo consecuencias nefastas en la calidad y realización del procedimiento de análisis. En ello se fundamenta la necesidad de realizar un estudio con el objetivo de describir la estabilidad de las muestras de sangre total empleando como anticoagulantes EDTAK2 y Heparina en el laboratorio de electroforesis de hemoglobina.
MÉTODOS
Se realizó un estudio descriptivo, en el cual se analizaron 100 muestras de sangre total de gestantes y sus respectivos esposos, que concurrieron al laboratorio de electroforesis de hemoglobina y laboratorio clínico del CNGM, durante los meses junio y julio de 2012, además de cinco muestras (controles comerciales que existen el laboratorio). El rango de edad de los pacientes estuvo entre 25 y 55 años (mujeres y hombres).
Las muestras fueron separadas de la identificación del paciente, añadidas a viales Eppendorf nuevos de 2mL y rotuladas por orden de llegada desde el número 1 al 100. Luego fueron conservadas a temperatura refrigerada (4-8 0C) y con 50 µL de los anticoagulantes más utilizados en este tipo de análisis (heparina y EDTA K2) y se analizaron por duplicado durante un mes, procesando las muestras a diferentes días. Para el estudio de estabilidad se analizaron las concentraciones de anticoagulantes: EDTA K2 al 10 % y heparina al 5 % y 2,2 %. Se realizaron corridas electroforéticas en gel de agarosa en el equipo Hydrasys, utilizando como referencia las cinco muestras de sangre de pacientes normales.
La estabilidad de la sangre se determinó observando la presencia de coágulos en los resultados de los datos obtenidos por duplicado y comparando la media de los resultados a los 7, 15 y 30 días de procesamiento de las muestras. Los parámetros establecidos como límites de aceptabilidad, fueron: a) ausencia de coágulos, b) limpieza en las corridas electroforéticas, c) buena migración de las bandas y d) buena interpretación de los resultados.
Los cambios fueron considerados significativos si la media de los resultados de cada día superaba el rango del límite de aceptabilidad.
RESULTADOS
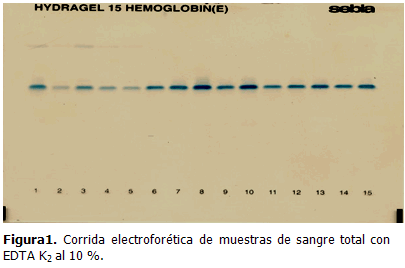
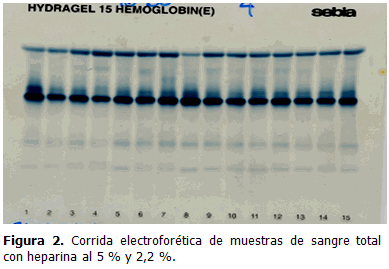
En el tiempo de estudio, las muestras procesadas con el anticoagulante EDTA K2 al 10 % no presentaron diferencias, observándose corridas electroforéticas con mayor exactitud y repetitividad. Los promedios de valores provenientes de muestras con heparina al 5 % presentaron problemas parciales con la coagulación y con heparina al 2,2 % todas las muestras se coagularon pasados dos días.
Las electroforesis realizadas a estas muestras heparinizadas presentaron restos de suciedad en las corridas, elevada concentración en la migración de las bandas y falsa interpretación de los resultados. En las figuras 1 y 2 se muestran las corridas electroforéticas realizadas a 15 muestras tratadas con los anticoagulantes estudiados.
DISCUSIÓN
En el presente trabajo se evaluó la conservación de la muestra con dos tipos de anticoagulantes teniendo en cuenta la estabilidad de la sangre a lo largo de un mes. Según la definición propuesta por Guder,5 la estabilidad de la muestra se basa en su capacidad para mantener los valores de sus propiedades biológicas dentro de límites preestablecidos bajo condiciones específicas. Los resultados obtenidos en estos ensayos pusieron de manifiesto diferencias en la coagulación de la sangre, dependiendo del anticoagulante y las respectivas concentraciones utilizadas.
Las muestras de sangre total trabajadas con heparina al 5 % para su empleo en electroforesis de hemoglobina a temperatura de 4-8 0C, podrían utilizarse por solo 3 días. No obstante, el riesgo de coagulación de la sangre es muy elevado, por lo que no se recomienda la conservación de la muestra con este anticoagulante durante periodos muy prolongados. En caso de utilizarse como anticoagulante, la heparina debe encontrarse al 5 % y en la proporción de 50 µL en 2 mL, para lograr una óptima calidad en las corridas electroforéticas y que no se degraden las muestras.
Al utilizarse el anticoagulante EDTA K2, la sangre permaneció estable durante el mes de estudio para todas las muestras. Este anticoagulante garantiza mayor seguridad, menos extracciones por punción venosa y mayor confiabilidad en los resultados. Además, actúa como agente quelante del calcio, lo que impide su activación y no deja producir la coagulación sanguínea.
Es uno de los anticoagulantes exógenos por excelencia, ya que cumple con varios requisitos para ser un buen anticoagulante por no alterar la morfología eritrocitaria ni leucocitaria; inhibe la aglutinación de plaquetas y asegura la conservación de elementos.6,7
Puede concluirse que el anticoagulante EDTAK2 al 10 % es el apropiado para garantizar la confiabilidad de los resultados en la pesquisa de hemoglobinopatías.
Debido a que cada laboratorio utiliza diferentes normas y tipos de anticoagulantes en dependencia del trabajo a desempeñar, es bueno resaltar que los resultados obtenidos en este trabajo puedan ser aplicables a todos los laboratorios clínicos, hematológicos y de electroforesis de hemoglobina.