INTRODUCCIÓN
El tratamiento del cáncer se basa actualmente en la quimioterapia antineoplásica. Los fármacos con mecanismo de acción citostático actúan de forma fundamental sobre las células en crecimiento, o produciendo daños sobre el ADN, lo cual provoca mecanismos de muerte celular o apoptosis. Sin embargo, este efecto no es específico frente al tumor, sino que se ejerce también sobre células progenitoras de todos los tejidos, produciendo una toxicidad limitante de la dosis. La administración de la terapia antineoplásica produce un descenso en la aparición de leucocitos en sangre periférica, alrededor de las 2 semanas, la cual apenas produce sintomatología excepto cuando aparece una infección.
La neutropenia y la infección son los efectos colaterales de la quimioterapia más limitantes de las dosis terapéuticas de mayor efectividad. La neutropenia se define por el número absoluto de neutrófilos en sangre menor de 1,5 x 109/L. El límite inferior normal es de 2,5 x 109/L y va disminuyendo fisiológicamente a lo largo de la infancia, pudiendo considerarse normal si las cifras son mayores de 1,5 x 109/L, tanto en niños de un año como en adultos sanos. Sin embargo, aproximadamente el 30 % de personas sanas de raza negra presentan cifras por debajo de ese rango y se consideran normales valores por encima de 1,0 x 109/L. (1,2)
La neutropenia puede originarse por alteraciones en la producción, maduración y/o distribución de neutrófilos, entre el compartimento circulante y el marginal, así como por destrucción periférica o por combinación de ambos mecanismos. Así mismo, según su intensidad puede clasificarse en leve (cuando el recuento de granulocitos neutrófilos es superior a 1 x 109/L, donde es poco probable que aparezcan síntomas infecciosos), moderada (cuando el recuento es de 0,5-1 x 109/L, aumenta el riesgo de padecer infecciones), y grave (cuando el recuento es inferior a 0,5 x 109/L y el riesgo de padecer infecciones severas es alto). No obstante, aunque las neutropenias graves tienen una predisposición mayor a las infecciones, se observa una gran variabilidad entre los distintos síndromes neutropénicos con recuentos leucocitarios similares, lo que sugiere que otros factores también determinan el riesgo infeccioso. (2-4)
El factor estimulante de colonias granulocíticas (G-CSF), es producido en muy pequeñas cantidades por el propio organismo. Sin embargo, el desarrollo de la tecnología de ADN recombinante ha permitido la producción de cantidades suficientes para su uso en pacientes neutropénicos. (5)
La Sociedad Americana de Oncología Clínica (ASCO) informa anualmente los resultados de investigaciones que continúan efectuándose internacionalmente y un grupo de expertos en G-CSF y otros estimulantes de colonias hematopoyéticas, de esa institución hace recomendaciones en sus guías de usos basadas en tales estudios. Ellos han señalado que no hay evidencias clínicas que justifiquen el uso de este medicamento en pacientes neutropénicos afebriles, sin embargo, advierten que es necesario esperar
Resultados de estudios más amplios que se están realizando en este sentido y exponen tres razones para valorar el uso del fármaco en estas circunstancias.
- Teóricamente el G-CSF activa los neutrófilos y puede ser más efectivo en la protección de la fiebre y contra el riesgo potencial de infección.
- Es posible que se acorte el período de neutropenia.
- Su uso en pacientes que reciben quimio o radioterapia se recomienda sólo cuando la intensidad del tratamiento combinado ocasiona mielotoxicidad, mucositis y neumonitis, pero lo contraindican en la irradiación del mediastino porque se produce trombocitopenia.
Actualmente se comercializa el G-CSF cubano conocido con el nombre de ior® Leukocim, producido en el Centro de Inmunología Molecular (CIM), lo cual posibilita el tratamiento de los pacientes con neutropenia después de la quimioterapia. Para la aprobación de su comercialización se realizaron estudios que avalan las indicaciones para las que se prescriben.(6)
No obstante, es necesario continuar con nuevas investigaciones en la práctica médica habitual para determinar si el producto es efectivo y seguro a las dosis recomendadas. Por ello, este trabajo tiene como objetivo evaluar la efectividad del iorâ Leukocim en profilaxis primaria, secundaria y episodios de neutropenia, en el curso del tratamiento con quimioterapia o radioterapia, en pacientes oncohematológicos de la provincia de Cienfuegos.
MÉTODOS
Se realizó un estudio de fase IV, multicéntrico, realizado en pacientes sometidos a quimio y/o radioterapia antineoplásica, a los cuales se les administró el factor estimulante de colonias granulocíticas (G–CSF), comercialmente denominado Leukocim y elaborado en el CIM.
En el estudio se incluyeron 95 episodios neutropénicos recogidos en historias clínicas y Cuadernos de Recogida de Datos (CRD), pertenecientes a 47 pacientes tratados en el Hospital ”Dr. Gustavo Aldereguía Lima” de Cienfuegos, durante el período comprendido entre enero de 2005 y enero de 2006.
Se analizaron las variables siguientes: sexo, color de la piel, tipo de indicación para el G-CSF, valores del conteo absoluto de neutrófilos (CAN) y del ácido úrico, número de dosis administradas, régimen de tratamiento y si hubo interrupción o no de este.
Criterios diagnósticos
Profilaxis primaria: En ciclos de quimioterapia (QT) con más del 40 % de episodios de neutropenia febril.
Profilaxis secundaria: En pacientes que hayan demorado la administración anterior de quimoterapia o radioterapia debido a prolongación de la neutropenia, o que hayan necesitado disminución de la dosis del citostático por esta causa.
En ambas indicaciones se aplicó el medicamento de 24 a 72 horas posteriores a la última sesión de quimioterapia o radioterapia recibida. La dosis diaria del fármaco fue de 300 g durante 7-10 días según criterio del investigador.
Su uso como tratamiento fue en pacientes con diagnóstico de neutropenia febril (CAN ≤1 x 109/L) o afebril (CAN ≤ 0,5 x 109 /L), en dosis de 300 g diarios por un período no mayor de 21 días hasta elevar las cifras del CAN a 1,5 X 109 /L o más.
Criterios de inclusión
- Pacientes que cumplan con el criterio diagnostico y/o condición de uso.
- Pacientes con diagnostico citológico y/o histológico de cáncer de cualquier localización que estaban recibiendo quimio o radioterapia.
- Pacientes mayores de 18 años que estén de acuerdo en recibir el producto.
Criterios de exclusión
- Pacientes con hipersensibilidad conocida a productos derivados de células de E. coli u otras preparaciones de ior G-CSF.
- Pacientes embarazadas o en período de lactancia.
Como variable principal de respuesta se consideró la administración del próximo ciclo de quimoterapia o radioterapia en el tiempo establecido. También se evaluó la corrección del CAN y tiempo en que fue recuperado.
RESULTADOS
La edad de los pacientes osciló entre los 17 y 81 años, con valor medio de 52 años. El 62,1 % pertenecían al sexo femenino y el 37,9 % al masculino. Hubo un predominio de los pacientes con color de la piel blanco con un 77,9 %, mientras que la piel mestiza se presentó en un 12,6 % y la negra en un 9,5 %.
La enfermedad base más frecuente fue la leucemia aguda no linfoblástica con un 34,7 %, seguida del linfoma no Hodgkin (15,8 %) y el Hodgkin (13,7%).
El 59,57 % de los pacientes presentó 1 episodio, seguido por un 14,89 % que tuvo 3, el 10,63 % manifestó 2 y el 8,51 % tuvo 4 eventos. Con 5, 7 y 8 episodios solamente hubo 1 paciente, para un 2,12 % respectivamente.
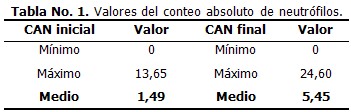
Como profilaxis primaria se indicó en el 8,4 % de los episodios, en el 31,6 % como secundaria y en el 60 % como tratamiento. El valor medio inicial del CAN fue 1,49 y el final 5,51. (Tabla 1)
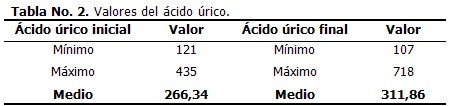
El valor medio inicial del ácido úrico fue 266,34 y el final 309,87. (Tabla 2)
En 9 episodios hubo interrupción del tratamiento (9,5%). En el 50,5 % de los casos (48) el tratamiento se aplicó de forma ambulatoria y en el 48,4 % (46) de forma intrahospitalaria. Sólo a 1 paciente no se le administró el medicamento.
El número medio de dosis administradas fue 6,69, con lo que se obtuvo la recuperación del CAN en una semana aproximadamente.
DISCUSIÓN
El uso del G-CSF ha permitido la administración de dosis efectivas de quimioterapia para el tratamiento de tumores quimiosensibles y un manejo adecuado de la toxicidad relacionada con las altas dosis de los medicamentos empleados. Se reportan datos de seguridad del tratamiento en diversas modalidades: dosis estándar de quimioterapia y altas dosis con o sin trasplante de progenitores hematopoyéticos. (4,7,8)
En la literatura consultada se señala elevación de leve a moderada, reversible y dosis dependiente del ácido úrico sérico, en pacientes sometidos a tratamiento con G-CSF (9,10). En nuestro estudio, los niveles del ácido úrico se monitorearon antes y después del uso del medicamento y en el 9,18 % se detectó hiperuricemia que desapareció una vez finalizado el tratamiento. Esto concuerda con estudios clínicos revisados, los cuales han demostrado buen perfil de seguridad y tolerancia. (10)