INTRODUCCIÓN
En 1845 John Hughes Bennett (1812-1875) tenía solamente 33 años y Rudolf Virchow (1821-1902) solamente 24, cuando cada uno describió, en necropsias, pacientes con dos características comunes: esplenomegalia y un cambio en el color y consistencia de la sangre. Aunque Bennett creyó que la sangre contenía material purulento, Virchow no se mostró conforme, por lo cual describió lo encontrado como sangre blanca o "leucemia", termino atribuido a él en 1847. (1)
En 1891 el premio Nobel Paul Ehrlich (1854-1915) lanzó nuevos métodos para teñir células sanguíneas y confirmó que los granulocitos eran el tipo de célula predominante en la forma mieloide de la leucemia. (1)
La clasificación francesa-americana-británica (FAB), divulgada en 1976, ha sido otro logro importante para un idioma universal entre hematopatólogos y hematólogos durante más de 30 años. Los avances en citogenética, inmunología, genética molecular y, más recientemente, la expresión de genes, han puesto cada vez más en claro la heterogeneidad de la leucemia aguda no linfoblástica (LANL), dando lugar a la nueva clasificación de las neoplasias mieloides de la OMS, reevaluada en el 2008. (2)
El progreso rápido en el conocimiento de la leucemia llevó al tratamiento clínico estándar de antraciclinas y Arabinosido de Citosina (Ara – C), desde 1982, en ciclos repetitivos consolidados por quimioterapia, curable para muchos pacientes con riesgos citogenéticos favorables e intermedios, pero con resultados muy modestos en los de alto riesgo y adultos mayores.(1)
El primer trasplante de médula ósea tuvo lugar en 1957, incorporándose desde entonces en los protocolos terapéuticos de las leucemias agudas. (3)
Las LANL son el resultado de la malignización de un precursor hematopoyético precoz, que provoca que esta célula dé lugar a una progenie que no es capaz de diferenciarse pero continúa proliferando de forma incontrolada, lo que trae como consecuencia la rápida acumulación de células mieloides inmaduras en la médula ósea. Estas células llamadas blastos, progresivamente reemplazan al tejido hematopoyético normal y provocan una reducción en la producción de las células normales de la sangre, que con el tiempo pasan al torrente circulatorio infiltrando el bazo, los ganglios, el hígado y otros órganos vitales. (4)
La mayoría de los tratamientos quimioterapéuticos han sido decepcionantes, con escasos resultados clínicos y elevados índices de mortalidad, por lo cual se hace necesaria la creación de nuevos protocolos de tratamiento, tal vez utilizando combinaciones de los diferentes agentes farmacológicos para lograr resultados más satisfactorios.(6)
Desde el comienzo del tratamiento de las LANL las antraciclinas y los análogos de las purinas (Citosar) han sido los pilares básicos del tratamiento. Sin embargo, en la actualidad los avances en la tecnología molecular, en la inmunohematología y en la farmacogenómica están abriendo nuevas luces en el tratamiento de estas enfermedades. (6)
Por otro lado un grupo grande de estudios aleatorios y controlados apoyan la hipótesis de que la solución terapéutica más viable en los pacientes jóvenes deben ser los regímenes que usan dosis más elevadas de los medicamentos convencionales, con alguna variante de trasplante. Sin embargo en los pacientes ancianos el propósito más razonable desde el punto de vista terapéutico sería la mejoría de la calidad de vida por encima de la posibilidad de una terapéutica curativa. (7)
En nuestro país en las bases de datos revisadas solo existen 3 estudios que hacen referencia a la epidemiología de las leucemias agudas, dos de series pediátricas, (8,9) una serie de morbimortalidad en adultos, (10) y un cuarto estudio que evalúa la frecuencia de la leucemia promielocítica ( LPM) en Cuba. (11)
Hasta el momento no se han realizado o publicado estudios a largo plazo, en cuanto a la sobrevida de las LANL en pacientes adultos en todo el país, razón por la cual se realizó esta investigación con el objetivo de caracterizar el comportamiento de la sobrevida de pacientes con leucemia aguda no linfoblástica en el Hospital “Dr. Gustavo Aldereguía Lima” de Cienfuegos.
MÉTODOS
Se realizó un estudio retrospectivo, analítico de series de casos en el Hospital General Universitario “ Dr. Gustavo Aldereguía Lima” de Cienfuegos, que incluyó a todos los pacientes a los que se le realizó diagnóstico de leucemia aguda no linfoblástica entre los años 1999 y hasta marzo del 2010 2010 en dicho hospital.
Se trabajó con todo el universo. Se analizaron las siguientes variables: edad según grupo de edades, sexo, variante morfológica de LANL, incidencia de LANL por año, sobrevida global, sobrevida global según sexo, sobrevida global según variante morfológica, sobrevida global según origen, sobrevida global según grupos de edades y sobrevida global según trasplante de médula ósea.
Los datos se extrajeron de los libros de registros de informes de medulogramas, de hemopatías malignas y las microhistorias individuales de cada paciente. Para su procesamiento se utilizaron los métodos de estadística descriptiva. Se calcularon además estadígrafos de tendencia central y de dispersión. Se aplicaron las pruebas estadísticas de Kaplan Meier para la estimación de la sobrevida.
Para el procesamiento y organización de la información se utilizó el paquete estadístico SPSS versión 12 para Windows. Los resultados se presentan en tablas y gráficos con números absolutos y porcentaje.
RESULTADOS
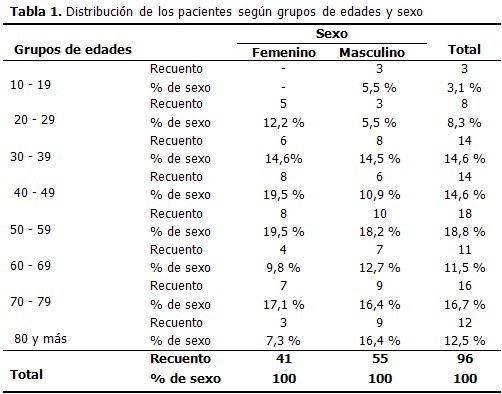
El mayor número de pacientes correspondió al sexo masculino con 55 casos, el resto fueron mujeres. El grupo de edades que mayor porcentaje aportó fue el comprendido entre los 50 a 59 años con 18,8 % de los casos, le siguieron en orden decreciente los comprendidos entre 70 a 79 con 16,7 % y los grupos entre 30 a 39 y 40 a 49 con 14,6 % en ambos casos. La edad media de la serie estudiada fue de 55 años con una desviación de 20 años. La tasa de incidencia estimada fue de 28,6 x 100 000 habitantes mayores de 15 años y el porciento de letalidad de las leucemias fue de 76,2 %. El paciente de menor edad tenía 15 años y el mayor 91.( Tabla 1).
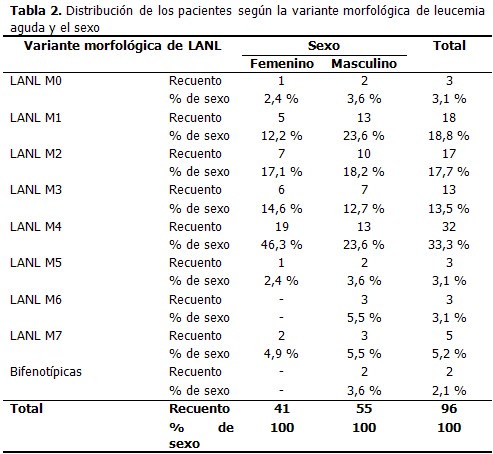
La variante morfológica más común de leucemia fue la mielomonocítica o M4 con 32 casos para 33, 3 % y en ella el sexo predominante fue el femenino. El resto de los subtipos no se comportó de la misma manera; en orden de frecuencia siguieron las variantes M1 y M2, las cuales fueron más frecuentes en el sexo masculino. (Tabla 2).
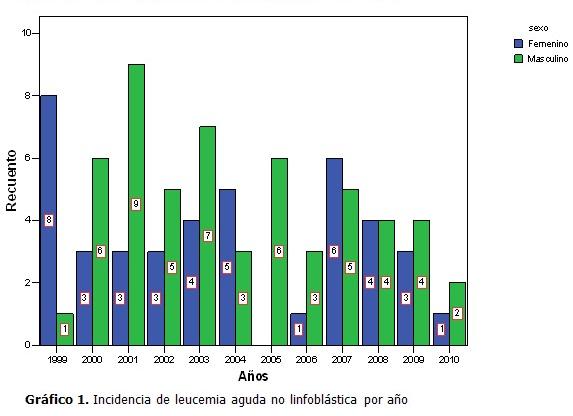
Se pudo comprobar que el año de mayor incidencia fue el 2001 con 12 casos, siguiendo en orden de frecuencia el año 2003 y 2007 con 11 pacientes cada uno. El resto de los años tuvo un comportamiento similar. (Gráfico 1).
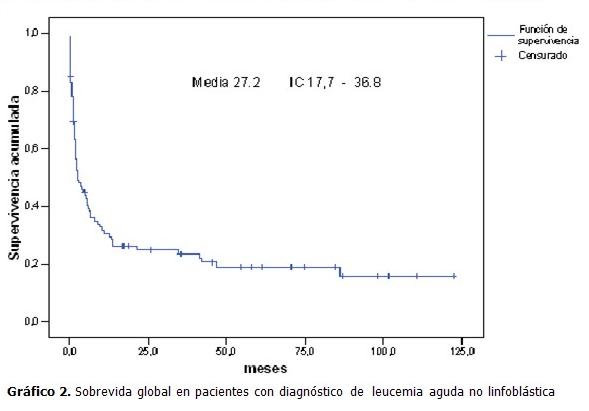
Al analizar la estimación de sobrevida global por el método de Kaplan Meier (12) se comprobó que fue de un 20 % para los 11 años de estudio. Del total de 96 pacientes, 77 están fallecidos y el resto vive. La media de supervivencia en meses fue 7 para los fallecidos y 54 en los que sobrevivieron. (Gráfico 2).
La sobrevida global por sexo durante los 11 años del estudio mostró que prácticamente no existen diferencias en la sobrevida para uno y otro sexo, con un valor p= 0, 4136.(Gráfico 3)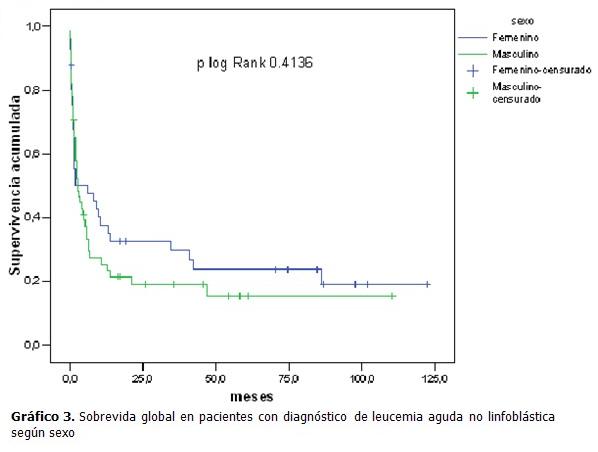
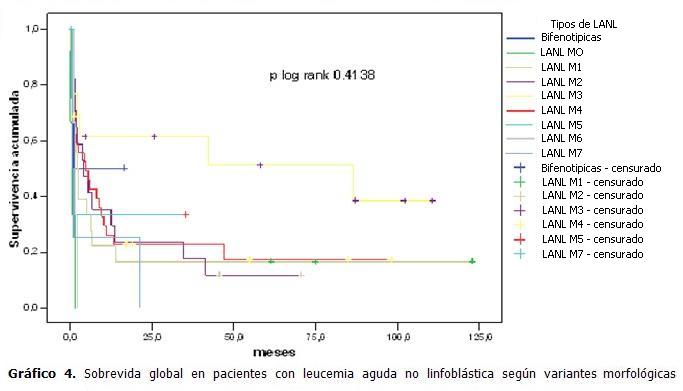
El análisis de la sobrevida global según la variante morfológica mostró que desde el punto de vista estadístico no existen diferencias en los distintos tipos de variantes morfológicas, sin embargo desde el punto de vista clínico la variante M3 tuvo mejores resultados a los 11 años de estudio con un 40 % de supervivencia. Y la de peor pronóstico resultó ser la variante M0. (Gráfico 4).
Al analizar la sobrevida de los pacientes de acuerdo al origen primario o secundario de la leucemia, se comprobó que las leucemias de origen secundario son de peor pronóstico, diferencia significativa desde el punto de vista estadístico ( p=0, 0015). (Gráfico 5).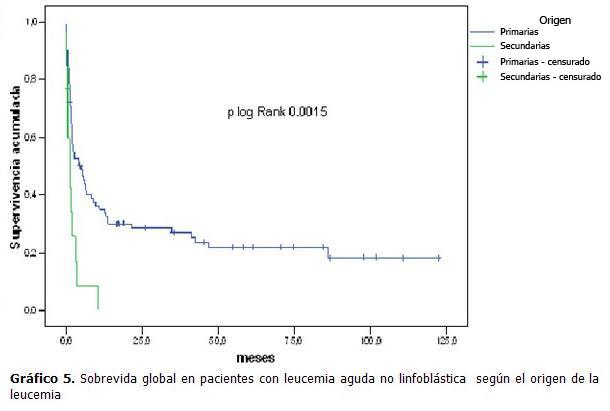
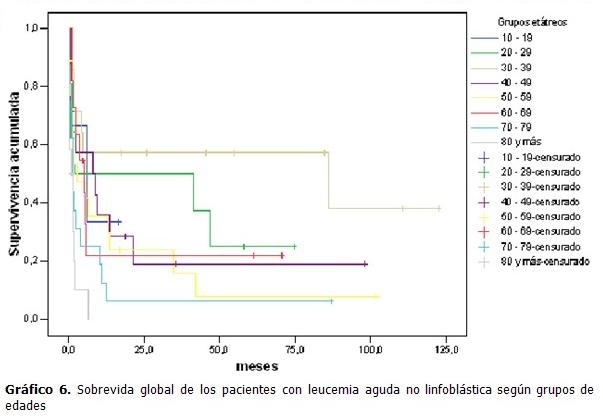
Tuvieron mejor sobrevida los pacientes con edades por debajo de los 40 años. (Gráfico 6).
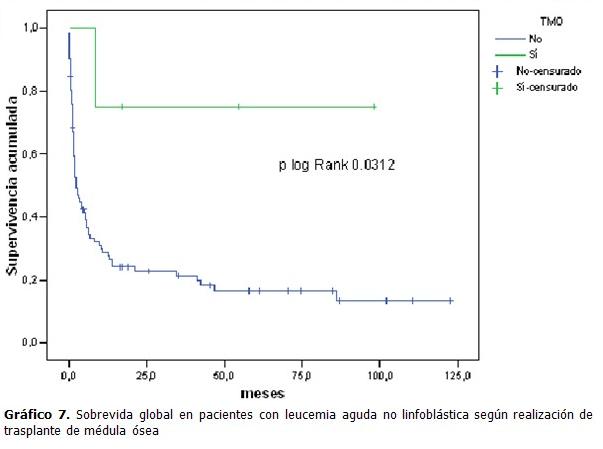
Se pudo comprobar que la sobrevida fue mayor en los pacientes a los que se les realizó trasplante de médula ósea, frente a aquellos que no la tuvieron, diferencia que resultó significativa desde el punto de vista estadístico ( p=0.0312). (Gráfico 7).
DISCUSIÓN
La leucemia mieloide aguda (LMA) es una enfermedad clonal heterogénea de las células progenitoras hematopoyéticas (“blastos”), los cuales pierden su habilidad de diferenciarse normalmente y de responder a los reguladores normales de la proliferación. Esta pérdida da lugar a una infección fatal, sangrado o infiltración de órgano, típicamente, en ausencia de tratamiento, durante el primer año del diagnóstico. (4)La LMA es la leucemia mieloide más común en la edad adulta, con una prevalencia de 3,8 casos por 100 000, que se eleva a 17,9 casos por 100 000 adultos en edades de 65 años o más. La edad promedio para su presentación está alrededor de los 70 años, a razón de tres hombres por cada 2 mujeres. En esta serie de casos, al igual que en otros estudios, el sexo predominante fue el masculino y la edad media de presentación fue menor que la habitualmente encontrada por otros autores. Sin embargo el mayor número de pacientes se sigue reportando en edades superiores a los 60 años, hecho que no entra en discordancia con lo reportado en la literatura. (13, 14)
En relación con la epidemiología de las leucemias agudas, la que con más frecuencia se reporta es la leucemia mielomonocítica o M4, en esta investigación también fue la variante morfológica más común. En orden de frecuencia le continúa la leucemia promielocitica o M3; de acuerdo a estudios epidemiológicos esta variante es la más frecuente en población hispánica. El comportamiento del resto de las variantes morfológicas es más o menos similar y el pronóstico es, por supuesto, más sombrío. (15)
La supervivencia global de los pacientes con LMA sigue siendo un reto para la mayoría de los grupos dedicados al estudio y tratamiento de esta enfermedad.(16) Los mejores resultados en cuanto a sobrevida global han sido reportados por un grupo pediátrico alemán, cuya filosofía de tratamiento se basa en un esquema bastante ordenado que emplea tres drogas en la inducción inicial, consolida con altas dosis de Citosar y emplea un esquema de intensificación tardía y finalmente uno de mantenimiento durante 12 a 24 meses; con ello logra una supervivencia a los 5 años de tratamiento de un 50 % por lo que la tendencia internacional ha sido tratar de extrapolar este esquema de tratamiento al adulto. (17)
Sin embargo los logros en sobrevida global del grupo del MD Anderson y el grupo del Instituto Nacional de Cáncer de los EE.UU. no han podido superar tasas superiores al 20 % en 5 años de estudio. Tampoco estos estudios han podido demostrar diferencias en cuanto a la sobrevida en relación con el sexo. (18)
Explicando de forma amplia este aspecto, los factores pronósticos se pueden dividir en aquellos asociados con la muerte relacionada con el tratamiento, que ocurre antes de que se alcance una respuesta, y aquellos asociados con la resistencia al tratamiento. El predictor principal de la muerte relacionada con el tratamiento es el estado del paciente en la escala de Zubrod. Edad, albúmina sérica, bilirrubina, creatinina y varios índices de morbilidad son otros predictores de la muerte temprana, de los cuales cada morbilidad es independiente de la otra, así como el estado de presentación.
Alrededor del 55 % de los adultos tienen alteraciones citogenéticas al diagnóstico. Los hallazgos citogenéticos permiten categorizar el riesgo del paciente como favorable, intermedio o adverso, con opciones de curación muy diferentes. Sin embargo, hay una variabilidad substancial en la respuesta, particularmente en los grupos favorables e intermedios.(19,20) La presencia de alteraciones cromosómicas secundarias sobreañadidas a la alteración primaria, mutaciones genéticas y expresión no controlada de genes son útiles para desentrañar esta heterogeneidad, así, ensayos clínicos realizados por el German LMA Intergroup (21, 22) y por el Cáncer and Leucemia Group B (23) han mostrado que la trisomía 22 mejora la sobrevida libre de recaída en la LMA asociada con inversión del cromosoma 16 (inv 16) y el grupo alemán también mostró que la ausencia de cromosoma Y está asociada con una sobrevida menor en hombres con la traslocación t (8;21). Como predijo el modelo de los dos pasos de la LMA, mutaciones en los genes RAS y el receptor de la tirosina kinasa son comunes en la LMA con t (8;21) e inv 16, y en tres series, las mutaciones KIT estaban asociadas con un inferior pronóstico. El antecedente racial también puede afectar la respuesta, en un estudio los pacientes no blancos con t (8;21) tenían una respuesta menor a la terapia de inducción, no siendo esta diferencia debida a una atención inferior. (24, 25)
El hallazgo citogenético más común en el grupo de pronóstico intermedio es un cariotipo normal. Muchos de estos pacientes tienen anormalidades citogenéticas en FLT3, NPM1, CEBPA, MLL, RAS, BAALC o EVI1. Entre el 28-34 % de los pacientes con LMA y cariotipo normal tiene una duplicación en tandem interna en el dominio juxtamembrana de FLT3, el cual está asociado de forma consistente con una respuesta pobre. Un grupo adicional de estos pacientes (10-25 %) tienen mutaciones dentro del lazo de activación del segundo dominio de la tirosina kinasa. (16, 26)
Un meta análisis reciente sugiere que estas mutaciones también afectan de forma negativa la sobrevida libre de recaída, aunque el British MRC Group señaló recientemente un efecto favorable. La mutación de un gen somático más común en la LMA está en el gen de la nucleofosmina, (27, 28) la cual causa localización citoplasmática más que localización nuclear de proteína. Entre el 48-64 % de los pacientes con LMA y cariotipo normal tienen mutaciones NPM1. Estudios recientes han encontrado que la sobrevida y el tiempo libre de recaída es mejor en pacientes con mutaciones MPN1 que no tienen duplicaciones de tandem internas en FLT3 que en los otros tres subgrupos. (22, 29)
Una limitación de esta investigación es no haber podido establecer los grupos de riesgo citogenéticos que establecen todos los estudios internacionales.(7) En este estudio la leucemia mieloide de mejor comportamiento en cuanto a sobrevida global resultó ser la variante M3 o LPM, esta variante es la única que consistentemente muestra un pronóstico distinto al resto de las leucemias después de la introducción de los agentes de diferenciación celular como el ácido retinoico, reporta tasas de supervivencia superiores al 70 %. El pronóstico del resto de las variantes no suele diferir notablemente, si bien ya se sabe que desde el punto de vista molecular la presencia de ciertas alteraciones citogenéticas como por ejemplo la inversión del cromosoma 16 en la leucemia mielomonocítica, la traslocación 8;21 en la variante M2 resultan ser de mucho mejor pronóstico en los pacientes que la poseen y de hecho esto marca una estratificación del riesgo inicial para cada paciente en particular. (21)
La LMA relacionada con la terapia o que surge después de un síndrome mielodisplásico (SMD) (30) es generalmente más resistente al tratamiento estándar que la LMA primaria. Esto se debe a que en la evolución de los SMD se acumula un gran número de mutaciones a nivel del ADN y la adquisición del gen de resistencia a multidroga (MDR) hace más difícil el efecto citotóxico de las distintas drogas quimioterapéuticas. Este estudio no difiere de este planteamiento, el comportamiento en cuanto a sobrevida de leucemias agudas secundarias fue muy sombrío. (15)
El tratamiento para los pacientes menores de 60 años consiste en quimioterapia citotóxica y se pueden curar entre el 20-75 % de los casos, en dependencia fundamentalmente de la citogenética de la célula leucémica. Sin embargo, la quimioterapia produce tal resultado en menos del 10 % de los pacientes de mayor edad debido a su incapacidad de sobrevivir al tratamiento y fundamentalmente por la asociación de la edad avanzada con las anomalías citogenéticas que involucran el cromosoma 5 y 7. Una mejor comprensión de la patogenia de la LMA ha permitido el desarrollo de terapias más eficaces particularmente para los pacientes de mayor edad. Lograr el éxito en el “ataque” de las numerosas variantes genotípicas de la LMA es el mayor desafío. (18, 31)
En este estudio no se difiere de estos planteamientos, el grupo de peor pronóstico fue el mayor de 60 años similar a lo reportado en la mayoría de las investigaciones.
En relación con el trasplante de médula ósea los distintos estudios han sido inconsistentes en demostrar su utilidad. El trasplante alogénico parece ser la opción más viable desde el punto de vista curativo en los pacientes con riesgo intermedio y alto, con una sobrevida global de 50 % a los 5 años de realizado este. La opción del auto trasplante no ha mostrado ventajas significativas en relación con los esquemas de quimioterapia estándares al comparar ambos grupos. (32-35)
De acuerdo con los resultados obtenidos en este trabajo podemos concluir que la sobrevida por leucemias agudas no linfoblásticas es muy modesta, con una supervivencia global del 20 % para los 10 años de estudio, lo cual no difiere del comportamiento de esta enfermedad en el resto de los países como Europa y América del Norte.
La LANL presentó un predominio en el sexo masculino, el grupo que mayor porcentaje de diagnósticos arrojó fue el comprendido entre los 50 y 59 años. Existe mejor sobrevida en los pacientes menores de 60 años así como también en aquellos pacientes que tuvieron la opción del trasplante de médula ósea.